弱电解质的电离水的电离PH计算
2025-01-24
第 1 页 共 2 页 水溶液中的离子平衡练习(一) 1、下物质分类组合正确的是 ( ) 2、下列关于电解质的说法正确的是 ( ) A、强电解质溶液的导电性一定比弱电解质溶液的导电性强 B、强电解质都是离子化合物,而弱电解质都是共价化 合物 C、强电解质在稀的水溶液中全 部以离子的形态存在 D、水溶液中导电能力差的电解质一定是弱电解质 3. 将氢氧化钠稀溶液滴加到醋酸稀溶液中,下列各图示意混合溶液有关量或性质的变化趋势,其中 错误..的是 ( ) NaOH滴加量 温度 A NaOH滴加量 pH B NaOH滴加量 导电能力 C NaOH滴加量 D 浓度 NaOH CH3COOH 4. 将 0.lmol· 1L 醋酸溶液加水稀释,下列说法正确的是( ) A. 溶液中 c(H +)和 c(OH - )都减小 B. 溶液中 c(H+)增大 C. 醋酸电离平衡向左移动 D. 溶液的 pH 增大
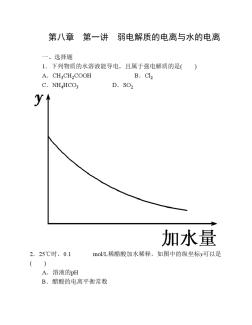
第八章第1讲弱电解质的电离与水的电离

第四讲弱电解质的电离和水的电离 考点一:电解质,非电解质,强、弱电解质的概念 1.根据你对电解质和非电解质的理解判断下列说法是否正确。 (1)电解质在水溶液中和熔融状态下都能导电() (2)固体氯化钠不导电,所以它不是电解质() (3)铜和石墨都能导电,它们都是电解质;cl2不能导电,故cl2是非电解质() (4)醋酸钠晶体不导电,醋酸钠溶液能导电,所以醋酸钠溶液是电解质,醋酸钠晶体是非电解质() (5)把so3溶于水所得的溶液能导电,所以so3是电解质() (6)baso4难溶于水,所以baso4是非电解质() 2.现有以下物质:①nacl晶体②液态hcl③caco3固体④熔融kcl⑤蔗糖⑥铜⑦co2⑧h2so4⑨koh固 体⑩盐酸。以上物质能导电的,以上物质属于电解质的是,属于非 电解质的是。 3.把0.05molnaoh固体分别加入到100ml
编辑推荐下载

弱电解质的电离平衡 [学情分析] 经过前面的学习,学生已经知道弱电解质的电离过程是一个可逆过程,并且最终建立电 离平衡,并且已经熟练掌握化学平衡的理论知识,已具备运用平衡理论解决实际问题的能力。 预计部分学生将会对浓度、外加物质对电离平衡的影响存在一定的困难,尤其是浓度变化对 弱电解质电离程度大小的影响感到难以理解。 [学习内容分析] 该部分知识主要包括“电离平衡常数”、“影响电离平衡的因素”两部分内容。该节所学“电 离平衡常数”与前面所学“化学平衡常数”、“水的离子积常数”,以及后面将要学习的“溶度积 常数”都属于平衡常数系列,可让学生对比学习,并为后面的学习埋下伏笔。在前面所学“外 界条件对化学平衡、水的电离影响”的基础上,学习“影响电离平衡的因素”更是水到渠成。学 好本节弱电解质电离平衡的知识,对下节分析溶液中各种离子间的作用,从而探究盐类水解 的

弱电解质的电离平衡 [学情分析] 经过前面的学习,学生已经知道弱电解质的电离过程是一个可逆过程,并且最终建立电 离平衡,并且已经熟练掌握化学平衡的理论知识,已具备运用平衡理论解决实际问题的能力。 预计部分学生将会对浓度、外加物质对电离平衡的影响存在一定的困难,尤其是浓度变化对 弱电解质电离程度大小的影响感到难以理解。 [学习内容分析] 该部分知识主要包括“电离平衡常数”、“影响电离平衡的因素”两部分内容。该节所学“电 离平衡常数”与前面所学“化学平衡常数”、“水的离子积常数”,以及后面将要学习的“溶度积 常数”都属于平衡常数系列,可让学生对比学习,并为后面的学习埋下伏笔。在前面所学“外 界条件对化学平衡、水的电离影响”的基础上,学习“影响电离平衡的因素”更是水到渠成。学 好本节弱电解质电离平衡的知识,对下节分析溶液中各种离子间的作用,从而探究盐类水解 的
热门文档 弱电解质的电离水的电离PH计算

第60讲弱电解质的电离及水的电离作业纸 1、下列关于强弱电解质的叙述错误的是 a.弱电解质在溶液中部分电离,存在电离平衡 b.在溶液中导电能力强的电解质是强电解质,导电能力弱的电解质是弱电解质 c.同一弱电解质的溶液,当温度、浓度不同时,其导电能力也不相同 d.纯净的强电解质在液态时,有的导电,有的不导电 2、在0.1mol·l -1 ch3cooh溶液中存在如下电离平衡:ch3coohch3coo - +h+对于 该平衡,下列叙述正确的是 a.加入水时,平衡向逆反应方向移动 b.加入少量naoh固体,平衡向正反应方向移动 c.加入少量0.1mol·l -1 hcl溶液,溶液中c(h +)减小 d.加入少量ch3coona固体,平衡向正反应方向移动 3、下列说法正确的是 a.向0.1mol·l -1 na2co3溶液中滴加酚酞,溶液变红色 b.al3+、no3 -

蒅弱电解质的电离平衡 肃命题趋向: 薈弱电解质电离平衡的考查主要是比较某些物质的导电能力大小,判断电解质非电解质;外界条件对电离平衡的影响及 电离平衡的移动;将电离平衡理论用于解释某些化学问题;同浓度(或同ph)强、弱电解质溶液的比较,如c(h+)大 小、起始反应速率、中和酸(或碱)的能力、稀释后ph的变化等等 袇【例1】判断下列说法中正确的是() 羃①氯气的水溶液导电,所以氯气是电解质。②二氧化碳的水溶液能导电,二氧化碳是电解质。③硫酸钡的水溶液不 导电,但是硫酸钡是电解质。④氯化钠溶液的水溶液能导电,氯化钠溶液是电解质。 袂a.①③b.③c.①③④d.都不正确 蚈二:强电电解质与弱电解质 芈3:强电解质: 蚅强电解包括的物质有: 蚁强电解质在水溶液存在的形式: 螈4:弱电解质:。 虿弱电解质包括的物质有: 膃弱电解质在溶液中存在的形式 蚄5:电离:电解:

1 第1讲弱电解质的电离平衡 [考纲解读]1.了解电解质的概念;了解强、弱电解质的概念。2.了解电解质在水溶液中的 电离以及电解质溶液的导电性。3.了解弱电解质在水溶液中的电离平衡。4.了解电离平衡常 数。 考点一强、弱电解质 1.电解质与非电解质 (1)电解质:在__________里或________状态下能导电的__________。 (2)非电解质:在水溶液里和熔融状态下____不能导电的____________。 2.强电解质和弱电解质 (1)概念 电解质 在水溶液里 (2)与化合物类型的关系 强电解质主要是大部分________化合物及某些________化合物。弱电解质主要是某些 ________化合物。 3.电离方程式的书写 (1)强电解质用______,弱电解质用________。 (2)多元弱酸分步电离,且第一步电离程

专题八溶液中的离子反应 基础课时1弱电解质的电离平衡 (时间:45分钟) 一、选择题(每小题仅有一个选项符合题意) 1.下列有关电解质的说法正确的是 ()。 a.强电解质的溶液一定比弱电解质的溶液导电性强 b.易溶性强电解质的溶液中不存在溶质分子 c.强电解质都是离子化合物,而弱电解质都是共价化合物 d.由于硫酸钡难溶于水,所以是弱电解质 解析溶液的导电能力与其中的离子浓度及离子所带电荷数多少有关,与溶质 是强电解质还是弱电解质无直接关系,a错;强电解质不一定都是离子化合物, 如hcl,c错;硫酸钡溶于水的部分能完全电离,是强电解质,d错。 答案b 2.已知h2so3、h2co3分别属于中强酸和弱酸,h2so3h++hso-3,hso-3 h++so2-3;h2co3h++hco-3;hco-3h++co2-3;电离平衡 常数分别为k1
精华文档 弱电解质的电离水的电离PH计算

lettersandcalls,anddopracticalthingsforthemassescombinegood,effectivethroughreachingpeopleattheserviceofthe"lastmile".third,fosterthedevelopmentofnewenergy,newgeneralsecretaryxijinpingstresseddevelopmentofinnovationforestrestructuring,revitalizationoftheoldindustrialbasesinnortheastchinaisthestate'smajorstrategy,centralha

教育资料 资料(一) 第八课时离子浓度大小比较跟踪训练 1.在1mol/lch3cooh溶液中下列关系不正确的是() a.c(ch3cooh)+c(ch3coo-)=1mol·l-1b.c(ch3cooh)>c(ch3coo-)>c(h+)>c(oh-) c.c(oh-)+c(ch3coo-)=c(h+)d.c(ch3cooh)>c(oh-)>c(ch3coo-)>c(h+) 2.在0.1mol/l的nh3·h2o溶液中,下列关系正确的是() a.c(nh3·h2o)>c(oh-)>c(nh4+)>c(h+)b.c(nh4+)>c(nh3·h2o)>c(oh-)>c(h+) c.c(nh3·h2o)>c(nh4+)=c(oh-)>c(h+)d.c(nh3·h2o)>c(nh4+)>c(h+

2019-2020学年高中化学第3章物质在水溶液中的行为第2节弱电解 质的电离盐类的水解学案鲁科版选修4 1.了解弱电解质的电离平衡常数概念和电离平衡常数与电离程度的关系。 2理解影响弱电解质电离平衡的因素及对电离平衡移动的影响。(重点) 3.了解常见弱酸和弱碱的电离常数大小,能比较它们的电离能力强弱。(难点) 电离平衡常数 教材整理1电离常数 1.定义:在一定条件下达到电离平衡时,弱电解质电离形成的各种离子的浓度的乘积 与溶液中未电离的分子的浓度之比是一个常数,这个常数称为电离平衡常数,简称电离常数。 2.表达式:一元弱酸:ch3coohch3coo-+h+ ka= [ch3coo-]·[h+] [ch3cooh] 一元弱碱:nh3·h2onh+4+oh- kb= [nh+4]·[oh-] [nh3·h2o]。 3.意义:电离常数

▁▂▃▄▅▆▇█▉▊▋▌精诚凝聚=^_^=成就梦想▁▂▃▄▅▆▇█▉▊▋▌ ▃▄▅▆▇██■▓点亮心灯~~~///(^v^)\\\~~~照亮人生▃▄▅▆▇██■▓ 四川省2012届高三化学第一轮复习《第10章第1讲弱电解质的电离平衡》同步练习 一、选择题(本题包括12个小题,每小题5分,共60分) 1.甲酸是一种一元有机酸。下列性质可以证明它是弱电解质的是() a.甲酸能与水以任意比互溶 b.1mol/l甲酸溶液的ph值约为2 c.10ml1mol/l甲酸恰好与10ml1mol/lnaoh溶液完全反应 d..甲酸溶液的导电性比盐酸溶液的弱 2.下列关于强弱电解质的叙述错误的是() a.弱电解质在溶液中部分电离,存在电
最新文档 弱电解质的电离水的电离PH计算
阐述了线性隔离放大器(线性光电耦合器)的工作原理,设计了线性隔离放大器的电离辐照试验,研究了线性隔离放大器的电离辐照效应,针对其结果进行了机理分析。

新型电解质锂盐主要包括含螯合硼阴离子、螯合磷阴离子、全氟膦阴离子、烷基磺酸阴离子、全氟烷基、亚胺基的有机锂盐及有机铝酸锂盐。本文综述了近年来在新型电解质锂盐研究与探索方面的成果,介绍了锂离子电池电解质锂盐的合成方法、组成与结构、化学和电化学性能及其与结构的关系,并阐述今后电解质锂盐研究的可能发展方向及研究方法。新型电解质锂盐主要包括含螯合硼阴离子、螯合磷阴离子、全氟膦阴离子、烷基磺酸阴离子、全氟烷基、亚胺基的有机锂盐及有机铝酸锂盐。本文综述了近年来在新型电解质锂盐研究与探索方面的成果,介绍了锂离子电池电解质锂盐的合成方法、组成与结构、化学和电化学性能及其与结构的关系,并阐述今后电解质锂盐研究的可能发展方向及研究方法。

研究了ni2+、cu2+、ca2+、mg2+等杂质离子对固体聚合物水电解槽性能的影响.在电解槽阳极室中分别加入这些杂质离子的硫酸盐,分析槽电压、阳极和阴极电势随时间的变化关系.结果显示杂质离子对电解槽有极大的损害.槽电压的迅速上升主要是由于阴极超电势的增加而造成.其原因是ni2+、cu2+在阴极催化剂与nafion膜的界面上沉积为金属,覆盖阴极催化剂,减小了反应活性位;而ca2+、mg2+则形成一层导电性差的氢氧化物膜,不但覆盖催化剂,减小了反应活性位,而且增加了阴极催化剂与nafion膜界面的接触电阻,导致阴极超电势的迅速增高.

文章研究ni%^2+、cu^2+、ca^2+、mg^2+等杂质离子对固体聚合物水电解槽性能的影响。在电解槽阳极室中分别加入这些杂质离子的硫酸盐,分析槽电压、阳极和阴极电势随时间的变化关系。结果显示杂质离子对电解槽有极大的损害。槽电压的迅速上升主要是由于阴极超电势的增加而造成,其原因是ni^2+、cu^2+在阴极催化剂与nafion膜的界面上沉积为金属,覆盖阴极催化剂,减小了反应活性位,而ca^2+、mg^2+则形成一层导电性差的氢氧化物膜,不但覆盖催化剂,减小了反应活性位,而且增加了阴极催化剂与nafion膜界面的接触电阻,导致阴极超电势的迅速增高。
设计了一种基于电离探测器的辐射源在线监测系统,该系统以嵌入式单片机为控制单元,以电离探测器为传感元件实现对辐射强度的监测,以gpsone模块实现对辐射源地理位置的监测和远程监控中心的通信。是一种集辐射量测量、辐射源定位、无线通信和报警等功能于一体的网络式辐射源在线监测系统。实验结果表明,该辐射源监测系统能够同时进行辐射源的强度测量和跟踪定位,辐射量测量精度为15%以内,室外定位精度在6m以内,室内定位精度在50m之内。

学生在学习人教版高中化学选修4《影响水的电离平衡因素》时,对于酸碱抑制水的电离、温度和易水解的盐促进水的电离熟记于心,而对于一类能与水发生反应的物质对水电离平衡的影响不甚清楚。大多教辅资料上面对上述问题也没有一个统一的看法,本文通过讨论高中阶段几种常见物质与水的反应,分析其微观机理。
绿色能源技术和低碳经济的发展对高性能锂离子电池提出了越来越高的要求。锂离子电池的发展主要依赖于电池材料的突破,而含氟材料因其结构稳定性好、安全性高而广泛应用。系统介绍了锂离子电池中涉及的含氟电极和电解质材料,着重对其应用特点和研究现状等进行了总结,并对锂电池相关含氟材料的发展方向进行了展望。

目的实现固体聚合物电解质水电解技术的工程化,解决这一技术在工程实施中存在的问题,使其满足密闭环境供氧设备的要求。方法电解池组采用阳极供水与压滤机组装的方式,针对水电解池供水与供电的要求,设计了电解池的极板以及集电板,并对极板进行了轻量化设计,组装了3套样机。结果在75℃、电流密度0.6a/cm2条件下,小池平均电解电压低于1.75v;在密闭舱内3人62d的试验考核中,水电解池堆运行稳定,产生的气体o2纯度高于99.5%;集成120个单电池的水电解器,能稳定输出压力为1mpa、流量为1523l/h的o2。结论水电解器的设计合理、极板轻量化设计可行,基本解决固体聚合物电解质水电解技术工程化应用中的技术问题,满足密闭环境对水电解器的性能要求。
综述了锂离子氧化物、硫化物玻璃及微晶玻璃固体电解质的研究进展。重点讨论了这些材料的电化学性能,以及离子掺杂对电化学性能的影响。探讨了锂离子玻璃和微晶玻璃固体电解质的发展及应用前景,认为其在全固态电池中的应用将随技术的发展实现商业化。
文辑创建者
我要分享 >
职位:岩土监测技术岗
擅长专业:土建 安装 装饰 市政 园林
相关编辑
文辑推荐
知识推荐
百科推荐

