锂空气电池
锂空气电池是一种用锂作阳极,以空气中的氧气作为阴极反应物的电池。锂空气电池比锂离子电池具有更高的能量密度,因为其阴极(以多孔碳为主)很轻,且氧气从环境中获取而不用保存在电池里。
放电过程:阳极的锂释放电子后成为锂阳离子(Li+),Li+穿过电解质材料,在阴极与氧气、以及从外电路流过来的电子结合生成氧化锂(Li2O)或者过氧化锂(Li2O2),并留在阴极。锂空气电池的开路电压为2.91 V。
-

选择特殊符号
选择搜索类型
请输入搜索
锂空气电池是一种用锂作阳极,以空气中的氧气作为阴极反应物的电池。锂空气电池比锂离子电池具有更高的能量密度,因为其阴极(以多孔碳为主)很轻,且氧气从环境中获取而不用保存在电池里。
放电过程:阳极的锂释放电子后成为锂阳离子(Li+),Li+穿过电解质材料,在阴极与氧气、以及从外电路流过来的电子结合生成氧化锂(Li2O)或者过氧化锂(Li2O2),并留在阴极。锂空气电池的开路电压为2.91 V。

锂空气电池这是一种由日本产业技术综合研究所与日本学术振兴会(JSPS)共同开发出的一种新构造的大容量锂空气电池。
理论上可实现大容量的"锂空气电池"作为新一代大容量电池而备受瞩目。不过此前的锂空气电池存在正极蓄积固体反应生成物,阻隔了电解液与空气的接触,导致停止放电等问题。
负极(金属锂)采用有机电解液,正极(空气)方面则使用水性电解液,两极由固体电解质隔开,以防止两电解液发生混合。由于固体电解质只通过锂离子,因此电池的反应可无阻碍地进行。正极的反应生成物具有水溶性,不产生固体物质。实验证明该电池可连续放电50000mAh/g(空气极的单位质量)。
该技术极有望用于汽车电池。如果在汽车用支架上更换正极的水性电解液,用卡盒等方式补充负极的金属锂的话,汽车可实现连续行驶且无需充电等待时间。可以从用过的水性电解液中轻松提取金属锂,锂能够反复使用。可以说是用金属锂作为燃料的新型燃料电池。
锂离子电池目前已经开始在电动汽车上应用,为了实现长距离行驶,作为蓄电池时的高性能化和低成本化备受期待。但目前的锂离子电池受制于电池容量很难实现长距离行驶,要实现长距离行驶必须在汽车上配备大量的电池,因此存在车体价格大幅上升的问题。
要实现电动汽车的普及,能源密度需达到目前的约6~7倍。因此,理论上能源密度远远大于锂离子电池的金属锂空气电池备受关注。由于锂空气电池的正极使用空气中的氧做活性物质,理论上正极容量无限大,因此可实现大容量。

大容量锂-空气电池并非新概念,至今都未普及原因是它存在致命缺陷,日本的研究院克服了这个困难,但 要想实现商用,可能还需要10年。减碳,对于人类福祉来说,绝对不是离谱的要求,但对于全球汽车业来说,却是一件困难的事情。
众所周知,锂离子电池广泛用于手机和笔记本电脑等,目前也已经是下一代充电式混合动力车和电动车的理想之选。它比其它汽车电池的密度更高、电量更充足,但也更贵,受制于电池容量,充电后的行驶距离仍不够远。即将于2010年上市的雪佛兰Volt混合动力汽车如果仅仅使用电池,只能行驶40公里。尽管仍有改进的空间,但锂离子电池的潜力依然有限。普遍认为,要实现电动汽车的普及,能源密度需达到目前的约6~7倍。于是,理论上能源密度远远大于锂离子电池的金属锂空气电池备受关注。虽然仍使用有机溶媒,但它却以全新的构成极大提高电池的能量密度。
锂-空气电池并非新概念。由于在正极上使用空气中的氧作为活性物质,理论上正极的容量密度是无限的,可加大容量。另外,如果负极使用金属锂,理论容量会比锂离子充电电池提高一位数。但是,为什么锂-空气电池至今都未普及?原因是它存在致命缺陷,即固体反应生成物氢氧化锂(LiOH)会在正极堆积,使电解液与空气的接触被阻断,从而导致放电停止。
2009年2月,日本产业技术综合研究所能源技术研究部门能源界面技术研究小组组长周豪慎和日本学术振兴会(JSPS)外籍特别研究员王永刚共同开发出了新构造的大容量锂空气电池。他们通过将电解液分成两种来解决上述问题。在负极(金属锂)一侧使用有机电解液,在正极(空气)一侧使用水性电解液。在两种电解液之间设置只有锂离子穿过的固体电解质膜,将两者隔开。这样便可防止电解液混合,并促进电池发生反应。
负极用电解液组合使用的是含有锂盐的有机电解液。虽然不能弃用有机溶媒,但却限定了使用方法。正极用水性电解液使用碱性水溶性凝胶,与微细化后的碳和低价氧化物催化剂形成的正极组合。在锂-空气电池中,由于放电反应生成的并非是固体的Li2O,而是容易溶解在水性电解液中的LiOH(氢氧化锂)。氧化锂在空气电极堆积后,不会导致工作停止。水及氮等也不会穿过固体电解质的隔壁,因此不存在与负极的锂金属发生反应的危险。而且,在充电时,如果配置充电专用的正极,还可防止充导电致空气电极的腐蚀和老化。
实验证明,以0.1A/g的放电率进行放电时,放电容量约为9000mAh/g,而以前的锂-空气电池的放电容量仅为700~3000mAh/g,可以说实现了容量的大幅增加。另外,如果使用水溶液取代水溶性凝胶,便可在空气中以0.1A/g的放电率连续放电20天,其放电容量约为5万mAh/g(空气极的单位质量),比原来高一位数。由于金属锂电池的容量原本就比锂离子电池高一位数,因此该数值共比锂离子充电电池高两位数。
现在,由于水溶液的性能较高,而在易用性上凝胶更为出色,科学家们今后需要考虑决定究竟对这两者中的哪一个进行开发。了解到,这种技术还可考虑与单纯的充电电池不同的使用方法。如果不对电池进行充电,而是通过汽车底座更换正极的水性电解液,以卡盒等方式补给负极的金属锂,汽车便可实现无需充电等待时间,立即行驶。而且,通过回收用过的水性电解液,以电气方式重新生成金属锂,还可继续作为电池负极燃料循环使用,避免产生其他污染。锂-空气电池可以说是以金属锂为燃料的新型燃料电池。
科学家认为,锂空气电池的性能是锂离子电池的10倍,可以提供与汽油同等的能量。锂空气电池从空气中吸收氧气充电,因此这种电池可以更小、更轻。全球不少实验室都在研究这种技术,但如果没有重大突破,要想实现商用可能还需要10年。

理论上,由于氧气作为阴极反应物不受限,该电池的容量仅取决于锂电极,其比能为5.21kWh/kg(包括氧气质量),或11.4kWh/kg(不包括氧气)。相对与其他的金属-空气电池,锂空气电池具有更高的比能(见下表) ,因此,它非常有吸引力。不过,锂空气电池仍在开发中,市场上还买不到。
金属/空气电池 | 理论开路电压(V) | 理论比能 (kWh/kg,含氧气) | 理论比能 (kWh/kg,不含氧气) |
Li/O2 | 2.91 | 5.210 | 11.140 |
Na/O2 | 1.94 | 1.677 | 2.260 |
Ca/O2 | 3.12 | 2.990 | 4.180 |
Mg/O2 | 2.93 | 2.789 | 6.462 |
Zn/O2 | 1.65 | 1.090 | 1.350 |
空气电池是化学电池的一种,其构造原理与干电池相似,所不同是它的氧化剂取自空气中的氧。目前空气电池主要有三大类即锌空气电池、锂空气电池和铝空气电池。
锌空气电池与其它传统电池相比,锌空气电池具有以下优点: 1 电池容量大. 空气电极工作正常的话,锌空气电池的理论容量是由负极活性物质的量决定的.负极(锌电极)位于电池内部,正极...
1、可重复使用圆柱形锌空气电池 2、一次性圆柱形锌空气电池 3、圆柱形锌空气电池 4、圆柱形锌空气电池 5、内氧式圆柱形锌-空气电池 6、圆柱形锌空气电池 7、一种用于圆柱形锌镍二次电池的组合盖帽 8...
日本产业技术综合研究所发布的锂空气电池的设计构思是,只在金属锂的负极使用有机电解液,正极的空气极使用水性电解液。既可以用作充电电池也可用作燃料电池使用。
如果在负极的有机电解液和空气极的水性电解液之间,用只能通过锂离子的固体电解质隔开的话,可防止两电解液发生混合,而且能促进电池发生反应。这样,能够防止正极的固体反应生成物--氧化锂(Li2O)析出。
该电池通过放电反应生成的不是固体氧化锂(Li2O),而是易溶于水性电解液的氢氧化锂(LiOH),这样就不会引起空气极的碳孔堵塞。另外,由于水和氮等无法通过固体电解质隔膜,因此不存在和负极的锂金属发生反应的危险。此外,配置了充电专用的正极,可防止充电时空气极发生腐蚀和劣化。
负极采用金属锂条,负极的电解液采用含有锂盐的有机电解液。中间设有用于隔开正极和负极的锂离子固体电解质。正极的水性电解液使用碱性水溶性凝胶,与由微细化碳和廉价氧化物催化剂形成的正极组合。
放电时电极反应如下:
(1)负极反应(Li→Li+e)
金属锂以锂离子(Li)的形式溶于有机电解液,电子供应给导线。溶解的锂离子(Li)穿过固体电解质移到正极的水性电解液中。
(2)正极反应(O2+2H2O+4e→4OH)
通过导线供应电子,空气中的氧气和水在微细化碳表面发生反应后生成氢氧根离子(OH)。在正极的水性电解液中与锂离子(Li)结合生成水溶性的氢氧化锂(LiOH)。
充电时电极反应如下:
(1)负极反应(Li+e→Li)
通过导线供应电子,锂离子(Li)由正极的水性电解液穿过固体电解质到达负极表面,在负极表面发生反应生成金属锂。
(2)正极反应(4OH→O2+2H2O+4e)
反应生成氧。产生的电子供应给导线。
使用了此次新开发的碱性水性电解质凝胶的锂空气电池在空气中以0.1A/g的放电率放电时,放电容量约为9000mAh/g。另外,充电容量也约达到9600mAh/g。与此前报道的原锂空气电池的容量(700~3000mAh/g)相比,放电容量大幅提高。而使用碱性水溶液代替碱性水溶性凝胶后,在空气中以0.1A/g的放电率放电时,可连续放电20天,放电容量约为50000mAh/g。
新的锂空气电池没电时也无需充电,只需更换正极的水性电解液,通过卡盒等方式更换负极的金属锂就可以连续使用。这是一种新型燃料电池,名为"金属锂燃料电池"。理论上30kg金属锂释放的能量与40L汽油释放的能量基本相同。如果从用过的水性电解液中回收空气极生成的氢氧化锂(LiOH),很容易重新生成金属锂,可作为燃料进行再利用。

在国家自然科学基金委、科技部和中科院等的大力支持下,中国科学院长春应化所张新波研究员带领的科研团队通过抑制锂-空气电池电解液分解,调控空气电极固-液-气三相界面以及优化锂-空二次电池体系与结构,成功将锂-空气电池循环寿命从目前文献报道的最长100次大幅提高至500次 。
针对目前锂-空气电池用电解液在电池反应中均有不同程度的分解,造成不可逆产物的生成和自身的消耗,严重限制电池循环寿命的难题,该团队基于对现有电解液分解机理的认识,首次将亚砜(DMSO)和砜(TMS)应用于锂-空气二次电池中,有效促进了可逆放电产物过氧化锂(Li2O2)的生成,减少了副反应;通过详细考察空气电极对锂-空气电池性能的影响,发现空气电极催化剂催化效率低、用于过氧化锂等不溶放电产物存储和反应物传输的孔道结构不合理、导电性差是制约锂-空电池性能的关键因素。基于此,该团队首次提出了石墨烯一体化空气电极的概念,成功地在泡沫镍基体中构筑了三维多孔石墨烯。泡沫镍所具有的高导电性,结合多孔石墨烯合适的孔道结构,使得所制备的锂-空气电池表现出优异的倍率性能;此外,通过借助和发挥稀土钙钛石型复合氧化物优异的电催化性能,有效降低了锂-空气电池充/放电过电位,进一步提高了能量转化效率和倍率性能。
在以上研究成果的基础上,还首次设计和开发出可实用化、拥有自主知识产权的锂-空气二次电池电池组。
剑桥大学研究人员开发出了锂-空气电池的实验室模型,解决了与相似的化学电池有关的数个问题。他们开发的锂-空气电池能量密度高,充电次数"超过2000次",能源使用效率理论上超过90%。

 有机电解液型锂空气电池空气电极研究进展
有机电解液型锂空气电池空气电极研究进展
有机电解液型锂空气电池空气电极研究进展
有机电解液体系的锂空气电池因其超高能量密度受到广泛关注.为寻求高性能、安全实用的锂空气电池,国内外就正极材料、催化剂、电解液和锂负极等开展了大量研究,其中空气电极的优化、电解液的稳定性是锂空气电池高性能发挥的关键.介绍了近年有机电解液锂空气电池空气电极上的反应机理、空气电极影响因素、正极材料和催化剂等最新研究进展,分析了各类多孔材料和催化剂的优缺点,及其对电池电化学性能的影响,结合本课题组研究成果,指出了锂空气电池空气电极的发展方向,即结合新型复合氧化物催化剂,构筑独特的多孔电极结构,以实现高容量、长寿命的锂空气电池.

 铝空气电池综述
铝空气电池综述
铝空气电池综述
铝空气电池综述 周荣灿 摘要:铝空气电池是实际比能量高达 300~400Wh/kg 且对环境非常友好的优秀电池;电池结构和使用的原材料可根 据实际环境和要求而变动,具有很大的适应性;它既可用于陆上又可用于深海,既可用作动力电池,又是长寿命高 比能的信号电池。 关键词 :铝电池;空气电池; Aluminum air battery Abstract:Aluminum/air(oxygen)fuel cell is one of long-life and high energy density batteries with actual specific energy reached 300-400 Wh/kg, and may be environment. Its structure and materials to be used may be determined accordi
可以订阅哦
据外媒报道,麻省理工学院(MIT)的研究人员与丰田欧洲研发团队的一位同事进行了缜密的测试,力图在一定程度上解决碘化锂(lithium iodide,LiI)电池材料及与锂-空气电池(lithium-air battery)相关的技术难题,例如:该材质难以维持多次充放电周期。但研究结果中存在矛盾之处,使研究人员对该材料的适用性产生疑问。尽管试验结果表明,该材料可能终究不是太适用,但该项研究为克服碘化锂材料的瑕疵及寻找替代性材料提供了指导意见。
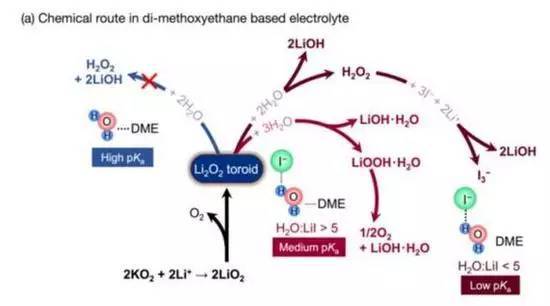
相较于锂离子电池,锂空气电池的工作原理不尽相同,锂离子与活性氧发生反应,在多孔电极(porous cathode)内部生成过氧化锂(lithium peroxide,Li2O2)聚合物。由于电极材料的容量难以容纳大量的过氧化锂,导致其比能量(specific energy)受限。
该团队采用不同方法,关注碘化锂在锂空气电池放电过程中所发挥的作用。他们随后又采用了紫外线光谱及可见光光谱(ultraviolet and visible-light spectroscopy)及其他技术研究电池的化学反应。在存在碘化锂及水的情况下,在上述研究进程过程中产生了氢氧化锂(lithium hydroxide,LiOH),而非过氧化锂。
碘化锂可提升水的反应性(reactivity),且更易损失质子(protons),促进了电池内氢氧化锂的形成,干扰了充电过程。据观察结果表明,研究团队已发现对相关化学反应的抑制方法,或能提升碘化锂等化合物的表现。
该研究论文的联合作者Graham Leverick表示:“该研究或将为选择碘化锂替代性化合物材料指明道路,有助于抑制电极表面不必要的化学反应。”
该项研究获得了丰田欧洲、Skoltech旗下电化学能量储存中心(Center for Electrochemical Energy Storage)的支持,其研究设备得到了美国国家科学基金会(National Science Foundation)的支持。来源:盖世汽车

据外媒报道,麻省理工学院(MIT)的研究人员与丰田欧洲研发团队的一位同事进行了缜密的测试,力图在一定程度上解决碘化锂(lithium iodide,LiI)电池材料及与锂-空气电池(lithium-air battery)相关的技术难题.
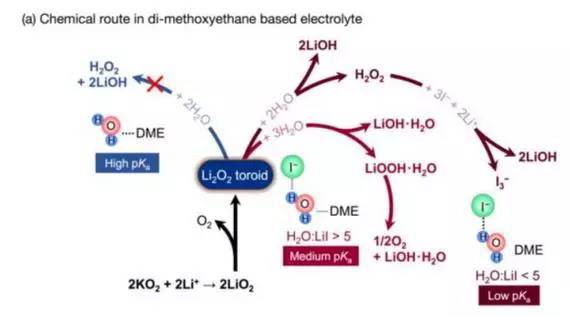
盖世汽车讯 据外媒报道,麻省理工学院(MIT)的研究人员与丰田欧洲研发团队的一位同事进行了缜密的测试,力图在一定程度上解决碘化锂(lithium iodide,LiI)电池材料及与锂-空气电池(lithium-air battery)相关的技术难题,例如:该材质难以维持多次充放电周期。
但研究结果中存在矛盾之处,使研究人员对该材料的适用性产生疑问。尽管试验结果表明,该材料可能终究不是太适用,但该项研究为克服碘化锂材料的瑕疵及寻找替代性材料提供了指导意见。
相较于锂离子电池,锂空气电池的工作原理不尽相同,锂离子与活性氧发生反应,在多孔电极(porous cathode)内部生成过氧化锂(lithium peroxide,Li2O2)聚合物。由于电极材料的容量难以容纳大量的过氧化锂,导致其比能量(specific energy)受限。
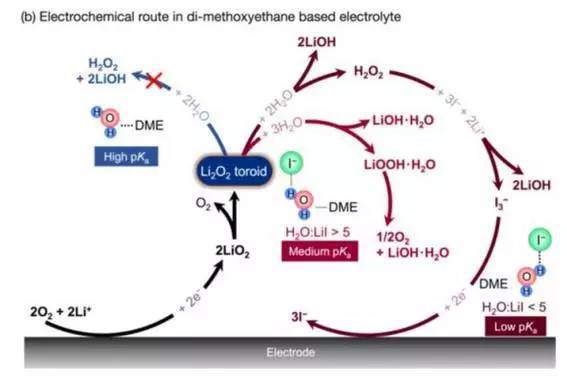
该团队采用不同方法,关注碘化锂在锂空气电池放电过程中所发挥的作用。他们随后又采用了紫外线光谱及可见光光谱(ultraviolet and visible-light spectroscopy)及其他技术研究电池的化学反应。在存在碘化锂及水的情况下,在上述研究进程过程中产生了氢氧化锂(lithium hydroxide,LiOH),而非过氧化锂。
碘化锂可提升水的反应性(reactivity),且更易损失质子(protons),促进了电池内氢氧化锂的形成,干扰了充电过程。据观察结果表明,研究团队已发现对相关化学反应的抑制方法,或能提升碘化锂等化合物的表现。
该研究论文的联合作者Graham Leverick表示:“该研究或将为选择碘化锂替代性化合物材料指明道路,有助于抑制电极表面不必要的化学反应。”
该项研究获得了丰田欧洲、Skoltech旗下电化学能量储存中心(Center for Electrochemical Energy Storage)的支持,其研究设备得到了美国国家科学基金会(National Science Foundation)的支持。
