绝热膨胀法测量空气的比热容比
(1)实验原理:
过程图如下:
I→II是绝热过程,由绝热过程方程得
状态I和状态III的温度均为T0,由气体状态方程得
合并式两式,消去V1、V2得
由上式可以看出,只要测得P0、P1、P2就可求得空气的绝热指数γ,即得到比热容比。
(2)实验仪器
(3)实验步骤
1、关闭放气阀A,打开充气阀B,用充气球向瓶内打气,使三位半数字电压表示值升高到100mV~150mV。然后关闭充气阀B,观察、的变化,经历一段时间后,指示值不变时,记下Po,此时瓶内气体近似为状态I。
2、打开放气阀。用气压计测定大气压强,用水银温度计测环境室温。开启电源,让电子仪器部件预热20分钟,然后旋转调零电位器旋钮,把用于测量空气压强的三位半数字电压表指示值调到“0”,并记录此时四位半数字电压表指示值。
3、迅速打开放气阀A,使瓶内气体与大气相通,由于瓶内气压高于大气压,瓶内∆V体积的气体将突然喷出,发出“嗤”的声音。当瓶内空气压强降至环境大气压强时(放气声刚结束),立刻关闭放气阀A,这时瓶内气体温度降低,状态变为II。
4、当瓶内空气的温度上升至温度T时,且压强稳定后,记下P2,此时瓶内气体近似为状态III。
5、记录室内大气压,根据P0、P1、P2,可以求出比热容比。
(4)注意事项
1、实验中贮气玻璃瓶及各仪器应放于合适位置,最好不要将贮气玻璃瓶放于靠桌沿处,以免打破。
2、转动充气阀和放气阀的活塞时,一定要一手扶住活塞,另一只手转动活塞,避免损坏活塞。
3、实验前应检查系统是否漏气,方法是关闭放气阀A,打开充气阀B,用充气球向瓶内打气,使瓶内压强升高1000Pa~2000Pa左右(对应电压值为20mV~40mV),关闭充气阀B,观察压强是否稳定,若始终下降则说明系统有漏气之处,须找出原因。
4、做好本实验的关键是放气要进行的十分迅速。即打开放气阀后又关上放气阀的动作要快捷,使瓶内气体与大气相通要充分且尽量快底完成。注意记录电压值。
振动法测定空气的比热容比
(1)实验原理
实验是通过测定小球在储气瓶玻璃管中的振动周期来测定空气的比热容比。
式中d为小球的直径,P为大气压强,T为室温,V为体积,m为小球的质量。
(2)实验仪器
(3)实验步骤
1.仪器调整
将气泵、储气瓶用橡皮管连接好,装有钢球的玻璃管插入球形储气瓶。将光电接收装置利用方形连接块固定在立杆上,固定位置于空芯玻璃管的小孔附近。 调节底板上三个水平调节螺钉,使底板处于水平状态。 接通气泵电源,缓慢调节气泵上的调节旋钮,数分钟后,待储气瓶内注入一定压力的气体后,玻璃管中的钢球离开弹簧,向管子上方移动,此时应调节好进气的大小,使钢球在玻璃管中以小孔为中心上下振动。
2、实验测量
设置:接通计时仪器的电源及光电接收装置与计时仪器的连接。打开计时仪器,预置测量次数为50次。(如需设置其它次数,可按“置数”键后,再按“上调”或“下调”键,调至所需次数,再按“置数”键确定。本实验按预置测量次数进行,不需要另外置数。)
测量:按“执行”键,即开始计数(状态显示灯闪烁)。待状态显示灯停止闪烁,显示屏显示的数字为振动50次所需的时间。重复测量5次。
其它测量
用螺旋测微计测出钢球的直径d,重复测量5次。
用物理天平称出钢球的质量m,左右盘各称一次。
3.记录室温和大气压和容器的体积;
根据公式求出空气的比热容比;
估算测量的不确定度。
(4)注意事项
若钢球不作简谐振动,可以调节气泵上面的气流调节阀门,直到钢球在玻璃管上小孔附近作稳定的谐振动。
接通电源后若不计时或不停止计时,可能是光电门位置放置不正确,造成钢球上下振动时未挡光,或者是外界光线过强,须适当挡光。
本实验装置主要系玻璃制成,且对玻璃管的要求特别高,振动钢球的直径仅比玻璃管内径小0.01mm左右,因此钢球表面不允许擦伤,在测量钢球质量和直径是要注意轻拿轻放,还要防止钢球表面粘上灰尘。2100433B

 空气比热容比的测量实验报告
空气比热容比的测量实验报告

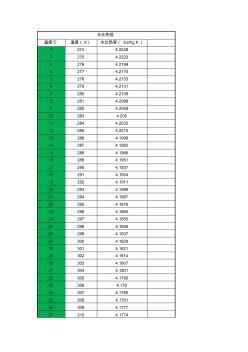 不同温度下水比热容
不同温度下水比热容