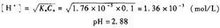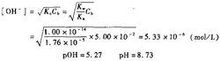化学计量点文献

 玻璃化学知识点总结
玻璃化学知识点总结
玻璃化学知识点总结
玻璃化学 第一章 1玻璃的定义 :玻璃是一种具有无规则结构的非晶态固体,其原子不像晶体那样 在空间作长程有序的排列,而近似于液体那样具有短程有序。 2玻璃的特性 :①各向同性 : 玻璃体在任何方向都具有相同的物理化学性质。 就 是说,玻璃态物质各个方向的硬度、弹性模量、热膨胀系数、热传导系数、折射 率、导电率等都是相同的, 而非等轴晶系的晶体具有各向异性。 ②介稳性玻璃处 于介稳状态,就是说,玻璃态物质是由熔融体过冷却或其它方法形成玻璃时, 系 统所含有的内能并不处于最低值③性质的可变性玻璃的成分在一定的范围内可 以连续变化,与此相应玻璃的性质也随之发生连续的变化。 ④性质变化的可逆性 :玻璃在固态和熔融态间可逆转化时,其物理化学性质的变 化是连续的和渐变的,而且是可逆的。 3玻璃的转变 :在 Tg~T 温度范围内及其附近的结构变化情况, 可以从三个温度 范围来说明: ①在 Tf 以上:由

 油田化学知识点总结
油田化学知识点总结
油田化学知识点总结
1、晶格取代 :在粘土矿物晶体中, 一部分阳离子被另外阳离子所置换,而晶体结构不变, 产 生过剩电荷的现象。 2、阳离子交换容量 : 分散介质 PH=7时, 1kg粘土所能交换下来的阳离子的毫摩尔数(以一价 阳离子毫摩尔数表示) 。 3、粘土造浆率 :一吨干粘土所能配制粘度(表观粘度)为 15mPa.s钻井液的体积数, m3/T。 4、钻井液碱度 : 用浓度为 0.01mol/L 的标准硫酸中和 1mL样品至酸碱中和指示剂变色时所需要 的体积(单位用 mL表示)。 5、钻井液触变性 : 一些非牛顿流体在机械作用下变稀(或变稠) ,在机械作用消除后则变稠 (或变稀)的性质。 6、塑性粘度 : Bingham流体流变曲线(直线)斜率的倒数。 7、钻井液的流变曲线 : 剪切应力与剪切速率之间的关系曲线。 8、流变模式 :表示流变曲线的数学式。 9、钻井液剪切稀释特性 : 钻井液表观粘度随剪切速率