物理性质
非金属单质大多是分子晶体,少部分为原子晶体和过渡型的层状晶体。
单质共价键数大部分符合8-N规则
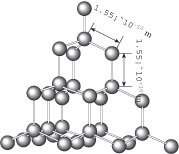
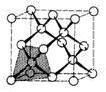
稀有气体:8-8=0(2-2=0),为单原子分子卤素,氢:8-7=1(2-1=1),为双原子分子VI A族的硫、硒、碲:8-6=2,为二配位的链形与环形分子V A族的磷、砷:8-5=3,为三配位的有限分子P4,As4,灰砷和黑磷为层状分子IV A族的碳、硅:8-4=4,为四配位的金刚石型结构。少数分子由于形成π键、大Π键或d轨道参与成键,键型发生变化,于是不遵守8-N规则。如N2、O2分子中的原子间的键不是单键;硼单质和石墨结构中,键的个数也不等于8-N个。
物理性质可分为三类
稀有气体及O2、N2、H2等:一般状态下为气体,固体为分子晶体,熔沸点很低多原子分子,S8、P4等:一般状态下为固体,分子晶体,熔沸点低,但比第一类高大分子单质,金刚石、晶态硅等:原子晶体,熔沸点高
化学性质
活泼非金属元素,如F2,Cl2,Br2,O2,P S等,能与金属形成卤化物、氧化物、硫化物,氢化物或含氧酸盐等。非金属元素之间也能形成卤化物、氧化物、无氧酸、含氧酸等。
大部分单质不与水反应,仅卤素与高温下的碳能与水发生反应。
非金属一般不与非氧化性稀酸发生反应,硼、碳、磷、硫、碘、砷等才能被浓硝酸、浓硫酸及王水氧化。
除碳、氮、氧外,一般可以和碱溶液发生反应,对于有变价的主要发生歧化反应;Si、B则是从碱溶液中置换出氢气;浓碱时,F2能氧化出O2
成键方式
非金属原子之间主要成共价键,而非金属元素与金属元素之间主要成离子键。
非金属原子之间成共价键的原因是,两种原子均有获得电子的能力,都倾向于获得对方的电子使自己达到稳定的构型,于是两者就共用电子对以达此目的。
而金属原子失去电子的能力较强,与非金属相遇时就一者失电子、一者得电子,双方均达到稳定结构。
多原子的共价分子常常出现的一种现象是轨道杂化,这使得中心原子更易和多个原子成键。
非金属原子之间形成的共价键中,除了一般的σ键和π键,还有一种大Π键。大Π键是离域的,可以增加共价分子或离子的稳定性。