选择特殊符号
选择搜索类型
请输入搜索
细胞静息时在膜两侧存在电位差的原因:①细胞膜两侧各种钠、钾离子浓度分布不均;②在不同状态下,细胞膜对各种离子的通透性不同。
枪乌贼轴突膜内外主要离子分布:
离子 | 细胞内液(mmol/L) | 细胞外液(mmol/L) | 能斯特电位(mV) |
钾离子 | 400 | 20 | -75 |
钠离子 | 50 | 440 | +55 |
氯离子 | 52 | 560 | -60 |
有机阴离子 | 385 | - | - |
细胞膜两侧的离子呈不均衡分布,膜内的钾离子高于膜外,膜内的钠离子和氯离子低于膜外,即胞内为高钾、低钠、低氯的环境。此外,有机阴离子仅存在于细胞内。在安静状态下,细胞膜对钾离子通透性大,对钠离子通透性很小,仅为钾离子通透性的1/100~1/50,而对氯离子则几乎没有通透性。因此,细胞 静息期主要的离子流为钾离子外流。钾离子外流导致正电荷向外转移,其结果导致细胞内的正电荷减少而细胞外正电荷增多,从而形成细胞膜外侧电位高而细胞膜内侧电位低的电位差。可见,钾离子外流是静息电位形成的基础,推动钾离子外流的动力是膜内外钾离子浓度差。
钾离子外流并不能无限制地进行下去,因为随着钾离子顺浓度差外流,它所形成的内负外正的电场力会阻止带正电荷的钾离子继续外流。当浓度差形成的促使钾离子外流的力与阻止钾离子外流的电场力达到平衡时,钾离子的净移动就会等于零。此时,细胞膜两侧稳定的电位差称为钾离子的电位。
根据物理化学能斯特公式,只要知道细胞膜两侧钾离子的浓度差,就可计算出钾离子的平衡电位。如果人工改变细胞膜外钾离子的浓度,当浓度增高时测得的静息电位值减小,当浓度降低时测得的静息电位值增大,其变化与根据能斯特公式计算所得的预期值基本一致。科学家注意到根据公式计算出钾离子平衡电位还是与实际测量出的静息电位有很小的一些差别的,测定值总是比计算值负得少。这是由于膜对钠离子和氯离子也有很小的通透性,它们的经膜扩散(主要指钠离子的内移),可以抵销一部分由钾离子外移造成的电位差数值。
静息状态下钾离子的外流是构成静息电位的主要因素。一般细胞内钾离子的浓度变化非常小,因此造成细胞内外钾离子浓度差变动的主要因素是细胞外的钾离子浓度。如果细胞外钾离子浓度增高,可使细胞内外的钾离子浓度差减小,从而使钾离子向外扩散的动力减弱,钾离子外流减少,结果是静息电位减小。反之,则使静息电位增高。这个实验也进一步说明,形成静息电位的主要离子就是钾离子。 这里的离子流动属于协助扩散,不消耗能量。

细胞膜两侧的电位差在某些情况下会发生变动,使细胞膜处于不同的电位状态。细胞安静时膜两侧内负外正的状态称为膜的极化状态。当膜电位向膜内负值增大方向变化时,称为超极化;相反,膜电位向膜内负值减小方向变化,称为去极化;去极化进一步加剧,膜内电位变为正值,而膜外电位变为负值,则称为反极化;细胞受到刺激后先发生反极化,再向膜内为负的静息电位水平恢复,称为膜的复极化。
静息电位是一种稳定的直流电位,但各种细胞的数值不同。哺乳动物的神经细胞的静息电位为-70mV(即膜内比膜外电位低70mV),骨骼肌细胞为-90mV,人的红细胞为-10mV。
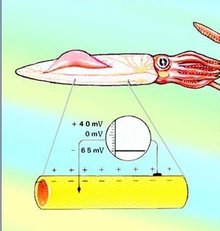
插入膜内的是尖端直径<1μm的玻璃管微电极,管内充以KCl溶液,膜外为参考电极,两电极连接到电位仪测定极间电位差。静息电位都表现为膜内比膜外电位低,即膜内带负电而膜外带正电。
因为神经轴突的中间部位是很长的一段结构相同的膜结构.当某点的电位变化后此点两端的膜内外离子出入的状态也是相同的. 就像你拿一条长导线,把中间一部分的绝缘皮去掉,从中间通电,两端都可测得电势差! 所以神...
晕死......初中化学貌似学习过的;石灰,与空气中的CO2 发生反应形成CACO3碳酸钙固化;熟石膏遇水吸水反应形成石膏固化,二水变一水结构。
破坏晶格的形成 比如碳酸钙 如果固体中少几个钙离子 那么他们就无法形成固体 大概就这个意思

 电网等电位操作机理及应用
电网等电位操作机理及应用
电网等电位操作机理及应用
依据相关技术规范要求,通过对变电站隔离开关开断状态下其两侧电压值的对比计算分析,揭示了等电位操作实质是变电站隔离开关在开断后、合闸前,其两侧所存在的电压,不会影响用该隔离开关安全转换电流的操作。通过隔离开关安全隔离故障断路器的实例,进一步说明深刻理解、灵活运用等电位操作机理的重要性。

 等电位_中间电位_地电位_原理
等电位_中间电位_地电位_原理
等电位_中间电位_地电位_原理
1、 变电站等电位接地的原理是什么? 答:等电位连接 (Equipotential bonding,bonding) :将分开的装置、诸导电物体用等电位连 接导体或电涌保护器连接起来以减小雷电流在它们之间产生的电位差。 在工程实践中,特别是自动化仪表工程,系统接地不但要防雷,而且要对意外的线路过 载、短路进行有效的安全保护, 更重要的是通过等电位连接来抑制电位差达到消除电磁干扰 的目的。这里的等电位连接导体,通常指工程现场俗称的 “接地网 ”。 等电位防雷器采用的元件为压敏电阻或放电管, 利用其电阻非线性原理, 以防止传输频率较 高并且容易受干扰的电子设备在接地时受到各种杂波干扰。 同时防止电子设备在接地时受到 地电位反击。 该防雷器在平时处于高阻状态, 与地网或等电位连接的其它设备和线路处于断 开状态, 一旦某局部出现高电位时它将在纳秒级迅速导通, 使通过它连接的各部分形成等电 位。等电
英文缩写:APD(action potential duration)
中文译名:动作电位时程
分类:医学
解释:(1)概念:可兴奋组织或细胞受到阈上刺激时,在静息电位基础上发生的快速、可逆转、可传播的细胞膜两侧的电变化。动作电位的主要成份是峰电位。
(2)形成条件:
①细胞膜两侧存在离子浓度差,细胞膜内K+浓度高于细胞膜外,而细胞外Na+、Ca2+、Cl-高于细胞内,这种浓度差的维持依靠离子泵的主动转运。(主要是Na+ -K+泵的转运)。
②细胞膜在不同状态下对不同离子的通透性不同,例如,安静时主要允许K+通透,而去极化到阈电位水平时又主要允许Na+通透。
③可兴奋组织或细胞受阈上刺激。
(3)形成过程:≥阈刺激→细胞部分去极化→Na+少量内流→去极化至阈电位水平→Na+内流与去极化形成正反馈(Na+爆发性内流)→达到Na+平衡电位(膜内为正膜外为负)(形成动作电位上升支)。
膜去极化达一定电位水平→Na+内流停止、K+迅速外流(形成动作电位下降支)。
(4)形成机制:动作电位上升支--Na+内流所致。
动作电位的幅度决定于细胞内外的Na+浓度差,细胞外液Na+浓度降低动作电位幅度也相应降低,而阻断Na+通道(河豚毒)则能阻碍动作电位的产生。
动作电位下降支--K+外流所致。
动作电位时细胞受到刺激时细胞膜产生的一次可逆的、可传导的电位变化。产生的机制为①阈刺激或阈上刺激使膜对Na+的通透性增加,Na+顺浓度梯度及电位差内流,使膜去极化,形成动作电位的上升支。②Na+通道失活,而 K+通道开放,K+外流,复极化形成动作电位的下降支。③钠泵的作用,将进入膜内的Na+泵出膜外,同时将膜外多余的 K+泵入膜内,恢复兴奋前时离子分布的浓度。
注 :动作电位时程(APD)即动作电位0-3相时程,此时心肌细胞对外界任何刺激均无反应,或只有局部反应(部分除极),故称为有效不应期(ERP ),期长短与APD变化一致
常用微电极有金属和玻璃两类,其电学性质不同,适用范围也略有差别。
金属微电极是一种高强度金属细针,尖端以外的部分用漆或玻璃绝缘。金属电极丝由不锈钢、铂铱合金或碳化钨丝在酸性溶液中电解腐蚀而成,有多种成品可供选择,其缺点是微电极的几何形状与绝缘状态难以保持一致。
玻璃微电极由用户根据需要用硬质毛细管拉制而成。用于测量细胞内静息电位和动作电位时,其尖端需小于0.5微米;用于测量细胞外活性区域非活性点电位时,其尖端可为1-5微米。
如图为单管玻璃微电极的结构示意图。在电极的粗端插入银-氯化银电极丝作为电气连接。玻璃微电极尖端内的电解液,与被测组织液之间形成了液体接触界面,界面的两侧离子迁移率和浓度不同,可以形成电位差。另一方面,由于电极尖端内径极小,因此形成高电极阻抗。通常选用3摩尔每升KCl溶液灌注玻璃微电极,用以减小电极阻抗。