
物理性质
无色,常温下为无色有刺激性气味的有毒气体,密度比空气大,易液化,易溶于水(约为1:40)密度2.551g/L。(气体,20摄氏度下)二氧化硫是一种主要的大气污染物。
熔点:-72.4℃(200.75K)
沸点:-10℃(263K)
溶解度:
| 22 g/100mL(0℃) | 15 g/100mL(10℃) |
| 11 g/100mL(20℃) | 9.4 g/100mL(25 ℃) |
| 8 g/100mL(30℃) | 6.5 g/100mL(40 ℃) |
| 5 g/100mL(50℃) | 4 g/100mL(60℃) |
| 3.5 g/100mL(70 ℃) | 3.4 g/100mL(80 ℃) |
| 3.5 g/100mL(90 ℃) | 3.7 g/100mL(100℃) |
化学性质
二氧化硫可以在硫磺燃烧的条件下生成
S(s) +O2(g) =点燃= SO2(g)
硫化氢可以燃烧生成二氧化硫
2H2S(g) + 3O2(g) =点燃= 2H2O(g) + 2SO2(g)
加热硫铁矿,闪锌矿,硫化汞,可以生成二氧化硫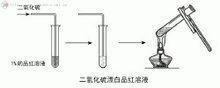 4FeS2(s) + 11O2(g) === 2Fe2O3(s) + 8SO2(g)
4FeS2(s) + 11O2(g) === 2Fe2O3(s) + 8SO2(g)
2ZnS(s) + 3O2(g) === 2ZnO(s) + 2SO2(g)
HgS(s) + O2(g) === Hg(g) + SO2(g)
应用:用于生产硫以及作为杀虫剂、杀菌剂、漂白剂和还原剂。在大气中,二氧化硫会氧化而成硫酸雾或硫酸盐气溶胶,是环境酸化的重要前驱物。大气中二氧化硫浓度在0.5ppm以上对人体已有潜在影响;在1~3ppm时多数人开始感到刺激;在400~500ppm时人会出现溃疡和肺水肿直至窒息死亡。二氧化硫与大气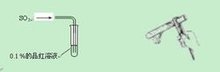 中的烟尘有协同作用。当大气中二氧化硫浓度为0.21ppm,烟尘浓度大于0.3mg/lL,可使呼吸道疾病发病率增高,慢性病患者的病情迅速恶化。如伦敦烟雾事件、马斯河谷事件和多诺拉等烟雾事件,都是这种协同作用造成的危害。
中的烟尘有协同作用。当大气中二氧化硫浓度为0.21ppm,烟尘浓度大于0.3mg/lL,可使呼吸道疾病发病率增高,慢性病患者的病情迅速恶化。如伦敦烟雾事件、马斯河谷事件和多诺拉等烟雾事件,都是这种协同作用造成的危害。
按照Claude Ribbe在《拿破仑的罪行》一书中的记载,二氧化硫在19世纪早期被一些在海地的君主当作一种毒药来镇压奴隶的反抗。
二氧化硫对食品有漂白(原理:与有色物质化合成无色不稳定物质)和防腐作用,使用二氧化硫能够达到使产品外观光亮、洁白的效果(特点:漂白不彻底),是食品加工中常用的漂白剂和防腐剂,但必须严格按照国家有关范围和标准使用,否则,会影响人体健康。国内工商部门和质量监督部门曾多次查出部分地方的个体商贩或有些食品生产企业,为了追求其产品具有良好的外观色泽,或延长食品包装期限,或为掩盖劣质食品,在食品中违规使用或超量使用二氧化硫类添加剂。
