碳酸钡
- 碳酸钡(Barium carbonate),是一种无机化合物,化学式为BaCO 3,为白色粉末,难溶于水,易溶于强酸,有毒,用途很广泛。
-

选择特殊符号
选择搜索类型
请输入搜索


中文名称:碳酸钡
英文名称:Barium carbonate
中文别名:C.I.颜料白10;碳酸钡;沉淀碳酸钡;毒重石;纳米碳酸钡;高纯碳酸钡;高纯碳酸钡BC-16;碳酸钡(1:1);颗粒碳酸钡;碳酸钡矿
英文别名:Barium carbonate
CAS号:513-77-9
分子式:BaCO₃
分子量:197.337
碳酸钡,化学式BaCO3,分子量197.336。白色粉末。难溶于水,密度4.43g/cm3,熔点881℃。1450℃分解,放出二氧化碳。微溶于含有二氧化碳的水,也溶于氯化铵或硝酸铵溶液生成络合物,溶于盐酸、硝酸放出二氧化碳。有毒。用于电子、仪表、冶金工业。配制焰火,制信号弹,陶瓷涂料,制光学玻璃的辅料。还用作杀鼠药、水澄清剂和填料。
是的
碳酸钡是难溶于水。没有物质是绝对不溶的,再难溶解的物质都会在水中或多或少溶解一点。只是习惯性把难溶物质成为不溶物质而已。难溶物的定义溶解度小于0.01g/100的都叫做难溶物。碳酸钡,化学式B...
可以碳酸氢钡化学式:Ba(HCO3)2弱碱性,易溶于水,难溶于乙醇,在100-120C分解生成碳酸钡,水和二氧化碳,由Ba(OH)2的80%乙醇溶液通入CO2或Ba(OH)2水溶液通入过量CO2可得:...
性状 工业品为白色粉末。
Melting_point 1740℃
相对Density 4.43
溶解性 几乎不溶于水,不溶于酒精,可溶于酸及氯化铵溶液。
有α、β、γ三种结晶状态。工业品为白色粉末。相对Density4.43。α-型Melting_point1740℃ (90.9×103Pa), 928 ℃时β-型转化为α-型,811℃时γ-型转化为β-型。几乎不溶于水,不溶于酒精,可溶于酸及氯化铵溶液。1450℃时分解而成氧化钡和二氧化碳。遇酸分解,与硫酸作用生成白色硫酸钡沉淀。微有吸湿性。有毒。
在硫化钡溶液中通入二氧化碳进行碳化,得到碳酸钡浆液。经脱硫洗涤、真空过滤、300℃下干燥、粉碎,制得碳酸钡成品。
BaS CO2 H2O=BaCO3 H2S
由硫化钡与碳酸铵进行复分解反应,再经洗涤、过滤、干燥等,即得碳酸钡成品。
BaS (NH4)2CO3=BaCO3 (NH4)2S
还可用氯化钡与碳酸钾反应制取:
BaCl2 K2CO3=BaCO3↓ 2KCl
将毒重石矿粉与铵盐反应生成可溶性钡盐,同时将碳酸铵回收使用,可溶性钡盐加入碳酸铵沉淀出精制碳酸钡,经过滤、干燥,制成成品。得到的母液可回收循环使用。
BaCO3 2HCl=BaCl2 H2O CO2↑
BaCl2 2NH4OH=Ba(OH)2 2NH4Cl
Ba(OH)2 CO2=BaCO3↓ H2O
储存注意事项[14] 储存于阴凉、通风的库房。远离火种、热源。包装密封。应与酸类、食用化学品分开存放,切忌混储。储区应备有合适的材料收容泄漏物。
用于陶瓷涂料和光学玻璃的辅料用于电子陶瓷、PTC热敏电阻、电容器等多种电子元器件的制造。分析钙、镁、锰和锌中的铁。检定和测定有机化合物中的卤素。用于制钡盐、颜料、焰火、杀鼠药陶器,并用作填料和水澄清剂等。用于催化剂。生产电子陶瓷及净化水,生产颜料、涂料或其它钡盐用于制光学玻璃、钡磁性材料等是生产显像管玻壳、磁性材料和高级光学玻璃的重要化工原料。处理镀铬电解液中过量的硫酸根,也用于镀锌层白色钝化溶液中,还可以用于处理含废水。
制法一:碳化法在硫化钡溶液(制备参见硫化钡)中通^二氧化碳气进行碳化,得到碳酸钡浆液经脱硫洗涤、真空过滤、300℃下干燥、粉碎,制得碳酸钡成品。其反应式如下:BaS+CO2+H2O→BaCO₃↓+H2S↑复分解法 由硫化钡与碳酸铵进行复分解反应,再经洗涤、过滤、干燥等,即得碳酸铋成品。其反应式如下:BaS+(NH4)2CO3→BaCO₃↓+(NH4)2S毒霞石转化法将毒重石矿粉与铵盐反应生成可溶性钡盐,同时将碳酸铵回收使用,可溶性钡盐加入碳酸铵沉淀出精制碳酸钡,经过滤、干燥,制得碳酸钡成品。得到的母液,经回收循环使用。
制法二:碳化法。反应方程式:BaS+CO2→BaCO₃↓+H2S↑ 操作方法:将1L含硫化钡180g/L的水溶液与二氧化碳在70℃反应,生成沉淀碳酸钡。沉淀用10ml 25%的氨水混合,在60℃脱硫20min。过滤、干燥后得沉淀碳酸钡,产品中含硫0.46%。复分解法。反应方程式:BaCl2+NH4HCO3+NH4OH→BaCO₃↓+2NH4Cl+H2O 操作方法:在30℃, 将23.6L含碳酸氢铵56.1g/L的水溶液与1.36L氨水在50L釜中混合,然后在50℃、在2h内滴加21.6L 200.3g/L的氯化钡溶液,在40℃搅拌30min。过滤,在140℃干燥,粉碎,得碳酸钡平均粒径d为0.8μm,纯度99.8%。毒重石法。反应方程式:BaCO₃+2NH4Cl→BaCl2+2NH3+H2O+CO2 BaCL2+(NH4)2CO3→BaCO₃↓+2NH4Cl 操作方法:将100g 80%的毒重石粉(120目)与60g氯化铵混匀,迅速放入650℃马弗炉中反应3min。冷却后水浸、过滤、除渣、得氯化钡溶液,加入36g碳酸铵,沉淀出碳酸钡,过滤、干燥、粉碎,转化率91%。
制法三:干法造粒将重质沉淀碳酸钡过筛,置于原料仓内充分搅拌、混合、脱气,物料经回转给料器、卧立式螺旋输送机输入辊压机辊压制片,制片厚度3.7~4 mm。将辊压成片的物料输入造粒机,通过调整其转速和筛板开孔大小来调整半成品的粒径分布。半成品采用刮刀式脉冲气力输送法将半成品经给料器输入至振动筛进行筛分,20目以上的颗粒送回造粒机,65目以下的微粒送回原料仓,65目至20目之间的颗粒输送到成品包装仓包装,制得颗粒碳酸钡。湿法造粒碳酸钡生产过程中由沉淀系统过滤分离后的含水滤饼,控制滤饼含水量在20%左右。在旋转桨叶的作用下,物料被迅速混合均匀,并得到混炼、捏合,形成密实的颗粒,将湿粒投入直接火回转窑内,在800~1200℃烧结。经整粒、筛选、脱铁、计量包装,制得颗粒碳酸钡。
碳酸钡是钡盐,有很强的毒性,碳酸钡会蓄积在骨骼上,引起骨髓造白细胞组织增生,从而发生慢性中毒。而且碳酸钡会与胃液中的盐酸发生反应,变成可溶性的氯化钡,氯化钡属于可溶性钡盐,为有毒物质,若不及时抢救,将会很快中毒,严重时会死亡。碳酸钡的LD50约418mg/kg。对碳酸钡急性中毒的患者,通常采取洗胃、灌肠、服用催吐剂等措施使碳酸钡排出体外。同时也可以通过服用硫酸钾与胃液中形成的可溶性氯化钡反应,能使有毒的钡变为不溶性硫酸钡沉淀,减轻毒性。之所以使用硫酸钾,是因为碳酸钡中毒可能会导致低血钾症。
1.主要用于生产PTC热敏电子元件、制造芯片式元器件、半导体电容等。2.分析钙、镁、锰和锌中铁,测有机物中的卤素。用于制钡盐、颜料、烟火和信号弹、光学玻璃、杀鼠药、陶器、瓷器,并用作填料和水澄清剂等。3.用作电子工业的原料,用于制备电容器、PTC电子元件、正温度系数热敏电阻等。4.用作分析试剂,焰火和信号弹燃料的配制,陶瓷涂料和光学玻璃的辅料。5.用于处理镀铬电解液中过量的硫酸根,也用于镀锌层白色钝化溶液中,还可以用于处理含铬废水。6.用作分析试剂、净水剂、杀鼠剂及制钡盐,也用于电子工业、仪器仪表、冶金工业。[15]
危险运输编码:UN 1564 6.1/PG 3
危险品标志:Xn
安全标识:S24/25
危险标识:R22
皮肤接触:脱去污染的衣着,用肥皂水和清水彻底冲洗皮肤。
眼睛接触:提起眼睑,用流动清水或生理盐水冲洗。就医。
吸入:迅速脱离现场至空气新鲜处。保持呼吸道通畅。如呼吸困难,给输氧。如呼吸停止,立即进行人工呼吸。就医。
食入:饮足量温水,催吐。用2%~5%硫酸钠溶液洗胃,导泻。就医。
CAS号:513-77-9
MDL号:MFCD00003448
EINECS号:208-167-3
RTECS号:CQ8600000
BRN号:7045119
PubChem号:24852112
危险特性:未有特殊的燃烧爆炸特性。
有害燃烧产物:一氧化碳、二氧化碳、氧化钡。
灭火方法:本品不燃。灭火剂:水、砂土。
应急处理: 隔离泄漏污染区,限制出入。建议应急处理人员戴防尘面具(全面罩),穿防毒服。不要直接接触泄漏物。小量泄漏:避免扬尘,用洁净的铲子收集于干燥、洁净、有盖的容器中。大量泄漏:用塑料布、帆布覆盖。然后收集回收或运至废物处理场所处置。
密闭操作,局部排风。操作人员必须经过专门培训,严格遵守操作规程。建议操作人员佩戴自吸过滤式防尘口罩,戴化学安全防护眼镜,穿防毒服,戴橡胶手套。避免产生粉尘。避免与酸类接触。搬运时要轻装轻卸,防止包装及容器损坏。配备泄漏应急处理设备。倒空的容器可能残留有害物。
疏水参数计算参考值(XlogP):无
氢键供体数量:0
氢键受体数量:3
可旋转化学键数量:0
互变异构体数量:0
拓扑分子极性表面积:63.2
重原子数量:5
表面电荷:0
复杂度:18.8
同位素原子数量:0
确定原子立构中心数量:0
不确定原子立构中心数量:0
确定化学键立构中心数量:0
不确定化学键立构中心数量:0
共价键单元数量:2
工程控制:密闭操作,局部排风。提供安全淋浴和洗眼设备。
呼吸系统防护:可能接触其粉尘时,必须佩戴自吸过滤式防尘口罩。紧急事态抢救或撤离时,建议佩戴空气呼吸器。
眼睛防护:戴化学安全防护眼镜。
身体防护:穿防毒服。
手防护:戴橡胶手套。
其他防护:工作现场禁止吸烟、进食和饮水。工作完毕,淋浴更衣。单独存放被毒物污染的衣服,洗后备用。保持良好的卫生习惯。
1.生态毒性 暂无资料
2.生物降解性 暂无资料
3.非生物降解性 暂无资料
1.稳定性[9] 稳定
2.禁配物[10] 强酸
3.避免接触的条件[11] 潮湿空气
4.聚合危害[12] 不聚合
5.分解产物[13] 氧化钡

 岩溶地区不整合地层系统地基评价——以贵州省天柱碳酸钡工程场地为例
岩溶地区不整合地层系统地基评价——以贵州省天柱碳酸钡工程场地为例
岩溶地区不整合地层系统地基评价——以贵州省天柱碳酸钡工程场地为例
岩溶地区不整合地层系统之岩土构成复杂。通过对贵州省天柱碳酸钡工程场地的勘察,选择卵(碎)石土层作地基持力层,采用浅基础方案及碎石层褥垫等地基处理措施,避让了岩溶等对地基稳定性的影响,为该地区的工程建设提供了岩土工程治理的经验。

 碳酸钠与碳酸氢钠性质的探究教学设计
碳酸钠与碳酸氢钠性质的探究教学设计
碳酸钠与碳酸氢钠性质的探究教学设计
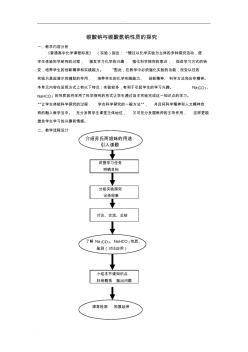
. . 碳酸钠与碳酸氢钠性质的探究 一、教学内容分析 《普通高中化学课程标准》 (实验)指出: “通过以化学实验为主体的多种探究活动,使 学生体验科学研究的过程, 激发学习化学的兴趣, 强化科学探究的意识, 促进学习方式的转 变,培养学生的创新精神和实践能力。 ”因此,在教学中必须强化实验的功能,改变以往的 实验只是起演示和辅助的作用, 培养学生的化学实践能力、 创新精神、 科学方法和合作精神。 本单元内容在呈现方式上有以下特点:实验较多,有利于引起学生的学习兴趣。 Na2CO3、 NaHCO 3 的性质我将采用了科学探究的形式让学生通过自主实验完成这一知识点的学习。 “让学生体验科学探究的过程, 学会科学探究的一般方法”, 并且将科学精神和人文精神自 然的融入教学当中。 充分发挥学生课堂主体地位, 又可充分发掘教师的主导作用, 这样更能 激发学生学习的兴趣和情感。 二、教学流程设计
碳酸钡是一种重要的基础无机化工原料,广泛应用于显像管、陶瓷、搪瓷、电容器、光学玻璃以及钡铁氧体。
由于碳酸钡具有较强的X射线屏蔽能力,将其加入显像管玻壳中可以有效吸收高压电流下产生的X射线;在结构陶瓷的生产中,添加粉状碳酸钡可以显著的提高瓷砖的硬度、耐磨性和耐化学腐蚀性;添加碳酸钡还可以提高釉料的耐摩擦性,同时色泽牢固光亮稳定;在玻璃制造方面,碳酸被用作培添加剂可以增加玻璃的可浇注性,同时可以显著提高玻璃的折射率、硬度和耐刻划性;超细碳酸钡粉体具有优异的磁学特性,用它制成的钡铁氧体具有高矫顽场强和磁学性能,已引起人们的重视。
随着科学技术的迅猛发展,电子化工等领域对碳酸钡的要求越来越高,而普通工业碳酸钡粉末的平均粒度在5μm以上,难以满足高科技领域发展的要求。与普通工业碳酸钡粉末相比,超细碳酸钡具有较高的介电系数、低耗能、高磁导率、饱和磁化强度等优点,具有潜在应用前景。近年来,人们一直进行利用各种方法制备抄袭碳酸钡粉体,并且将其应用于实际生产,初步取得了一定的成效,单人存在许多问题,例如对设备要求高,成本高,生产效率低,产品质量不稳定。因此,对超细碳酸钡制备方法及应用的研究和探索成为研究的热点。具有高矫顽场强和磁学性能,已引起人们的重视。
结构分类
天然碳酸钡
类别:碳酸盐(Carbonates),遇酸发泡
化学成分:BaCO3
晶系:斜方晶系(Orthorhombicsystem)2/m2/m2/m,晶体通常以(110)为双晶面,以三个单晶互生之形式,形成假六方双锥面,锥面上常有深的平行条纹,形成凹角 物理性质
硬度:3.5
水溶性:难
断口:参差状(Uneven)
条痕:白色
常见型态:葡萄状、球状、柱状、粒状、晶体通常为双面晶
常见光泽:玻璃光泽、断口油脂光泽
常见颜色:无色、灰色、白色,黑色,
常见比重:3.5-4.
基本用途
毒重石是除重晶石(BaSO4)外,自然界另一种主要含钡矿物。具有比重大、硬度低、吸收X射线和γ射线等特性,广泛应用于油气钻探、化工、轻工、冶金、建材、医药等工业部门,特别是化工产品制造中的优质钡原料。

碳钡矿过去叫毒重石或碳酸钡矿,它是一种碳酸盐矿物。碳钡矿分布很稀少,但它却是钡的次要矿石(钡的主要矿石资源是重晶石)。碳钡矿的晶体集合体可为块状、球状、肾状、纤维状或葡萄状。颜色为白、灰、浅黄等色,具有玻璃光泽,在阴极射线照射下会发出浅蓝色的荧光。