选择特殊符号
选择搜索类型
请输入搜索
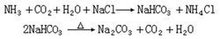
碳酸盐的制备方法有以下四种:
①氨碱法:
② 碱吸收二氧化碳法:
2NaOH+CO2─→Na2CO3+H2O
2NH3+CO2+H2O─→(NH4)2CO3
③ 可溶性碳酸盐沉淀难溶碳酸盐法:
Na2CO3+CaCl2─→CaCO3+2NaCl
④ 酸式碳酸盐热分解沉淀法:
'
酸式碳酸盐通常可用碳酸盐进一步吸收二氧化碳的反应制备:
Na2CO3+CO2+H2O─→2NaHCO3
也可用碱吸收过量二氧化碳制备:
KOH+CO2─→KHCO3
NH3+H2O+CO2─→NH4HCO3
此外,难溶的碱式碳酸盐可由某些金属的可溶性盐类溶液中加入碱金属碳酸盐溶液来制备:
式中M为Be、Mg、Cu等。
应用 在碳酸盐中,纯碱(碳酸钠)是重要的化工原料,广泛应用于化工、玻璃、肥皂、造纸、纺织和食品等工业。钾碱(碳酸钾)是玻璃生产的主要原料。小苏打(碳酸氢钠)广泛用于医药和食品工业,也常用于制造灭火器。石灰石、大理石、白云石可用于建筑、水泥和钢铁等工业。
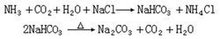
碳酸盐和酸式碳酸盐大多数为无色的。碱金属和铵的碳酸盐易溶于水,其他金属的碳酸盐都难溶于水。碳酸氢钠在水中的溶解度较小,其他酸式碳酸盐都易溶于水。碱式碳酸盐一般难溶于水。
关于碳酸盐在水中的溶解性,一般来说,碳酸盐难溶的金属,碳酸氢盐溶解度相对较大;而碳酸盐易溶的金属,碳酸氢盐的溶解度则明显减小。普遍认为是HCO3-离子在溶液中形成了氢键相互缔合,使溶解度减小的缘故。可溶性碳酸盐在水溶液中都会水解,使溶液呈碱性。如0.1Μ碳酸钠溶液的pH为11.6,其溶液中存在分步水解平衡:
其中第一步水解是主要的。对于碱金属的酸式碳酸盐来说,第二步是主要的,但水解程度远小于第一步。另外,HCO婣还要电离。因而0.1Μ碳酸氢钠水溶液呈弱碱性,pH为8.3。
难溶于水的碳酸盐都能溶于稀的强酸、乙酸或二氧化碳的饱和溶液中,例如: 碳酸盐在加热时都会分解成金属氧化物并放出二氧化碳,此反应为非氧化还原反应。(对于碳酸银,加热后由于Ag2O不稳定,即分解为单质银和氧气。)不同碳酸盐的热稳定性差异很大。其中碱金属和碱土金属碳酸盐的热稳定性较高,必须灼烧至高温才分解;而有些金属的碳酸盐的热稳性较低,加热到100℃左右就分解,如碳酸铍等;有的碳酸盐在常温下就可以分解,如碳酸汞。酸式碳酸盐的热稳定性比相同金属的碳酸盐低得多。例如碳酸钠,要851℃以上才开始分解,而碳酸氢钠在270℃左右就明显分解:
酸式碳酸盐的溶液在常温下会缓慢放出CO2而分解。
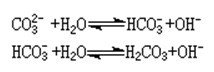
化学式:ZnCO3
外观:白色粉末、无毒、无味。
用途:可用于生产人造丝、化肥行业的脱硫剂、催化剂的主要原料,在橡胶制品、油漆其它化工产品中也可广泛应用,在石油钻井中,本品能与HS反应生成稳定的不溶性ZnS,且该品加入泥浆后不影响泥浆性能,因而可有效的消除HS的污染和腐蚀,用作含HS油气井的缓蚀剂,除硫剂。
在碳酸盐中,纯碱(碳酸钠)是重要的化工原料,广泛应用于化工、玻璃、肥皂、造纸、纺织和食品等工业。钾碱(碳酸钾)是玻璃生产的主要原料。小苏打(碳酸氢钠)广泛用于医药和食品工业,也常用于制造灭火器。石灰石...
碱金属和碱土金属碳酸盐显碱性。碳酸铵显中性。
不能溶于水的碳酸盐显中性;能溶于水的碳酸盐中,如果是强碱与碳酸生成的盐就显碱性,如:碳酸钠、碳酸钾等强碱弱酸盐,只有碳酸根离子水解,所以显碱性。CO32-+H2O=HCO3-+OH-(可逆)HCO3-...
用标准盐酸溶液滴定水样时,若以酚酞作指示剂,滴定到等当点时,pH为8.4, 此时消耗的酸量仅相当于碳酸盐含量的一半,当再向溶液中加入甲基橙指示剂,继续滴定到等当点时,溶液的ph值为4. 4,这时所滴定的是由碳酸盐所转变的重碳酸盐和水样中原有的重碳酸盐的总和,根据酚酞和甲基橙指示的两次终点时所消耗的盐酸标准溶液的体积,即可分别计算碳酸盐和重碳酸盐的含量。
A salt of carbonic acid in which one hydrogen atom has been replaced; an acid carbonate.
含有两个碳酸根的盐类.
碳酸盐是金属元素阳离子和碳酸根相化合而成的盐类。碳酸盐矿物的种数在95种左右,其中白云石是在自然界分布极广的矿物,而且不少碳酸盐矿物是重要的非金属矿物原料,也是提取Fe,Mg,Mn,Cu等金属元素及放射性元素Th、U的重要矿物来源,具有重要的经济意义。 在碳酸盐矿物中,主要的阴离子为[CO3]2-,阳离子主 要是Ca2+、Mg2+,其次Na+、Fe2+以及Cu2+、Zn2+、Pb2+、Mn2+、Bi3+等。一些碳酸盐矿物具有完好的单晶体,也可呈块状、粒状、放射状和土状等集合体形态。 碳酸盐矿物大多数为无色或白色,含铜者呈鲜绿或鲜蓝色,含锰者呈玫瑰红色,含稀土者或铁者呈褐色,含钴者呈淡红色,含铀者呈黄色。矿物硬度不大,一般在3左右。最大的是稀土碳酸盐矿物的硬度,但也不超过4.5,非金属光泽为主。碳酸盐矿物主要为外生成因,分布广泛,可形成大面积分布的海相沉积地层。内生成因的碳酸盐岩多数出现在岩浆热液阶段。

英文翻译:basic carbonate(s)
属于碳酸盐的一种,是含有氢氧基团的金属离子碳酸盐。碳酸H2CO3的碱式盐,为复盐
重要的有碱式碳酸铜[CuCO3·Cu(OH)2]、碱式碳酸铅[2PbCO3·Pb(OH)2]等及自然界存在的蓝铜矿[Cu3(CO3)2(OH)2]、孔雀石[Cu2(OH)2CO3]等。
对比古生代和中生代世界缓坡碳酸盐沉积体系与生物礁和浅滩镶边的碳酸盐陆架沉积体系,两者的区别是,①缓坡碳酸盐沉积物表面坡度极小; 而镶边陆架碳酸盐沉积物表面则存在明显坡折。②缓坡不存在生物礁。③缓坡近岸内坡相碳酸盐产率比镶边陆架台地顶部少。④海平面略有下降时,缓坡相带向海盆方向迁移,不会同时完全暴露,而镶边陆架的台地表面会全部暴露。⑤当海泛缓慢发生时,缓坡不会象镶边陆架的台地那样突然被海水淹没,而是被缓慢逐渐淹没,有利于潜水面的不断上升,使泥炭沼泽环境得以长期持续,形成厚煤层甚至巨厚煤层;而易被海水突然淹没的镶边陆架上则很难形成厚煤层。
碳酸盐岩是自然界中重碳酸钙溶液发生过饱和, 从水体中沉淀形成。现代和古代碳酸盐沉积主要分布于低纬度带无河流注入的清澈而温暖的浅海陆棚环境以及滨岸地区。这是因为碳酸盐过饱和沉淀需要排出CO2,海水温度升高和海水深度变小都有利于水中CO2分压降低,促进重碳酸钙过饱和沉淀。另外,温暖浅海环境,生物发育,藻类光合作用均需要吸收CO2,也促进CaCO3的饱和和沉淀。底栖和浮游生物还通过生物化学和生物物理作用直接建造钙质骨骼,形成生物碳酸盐岩。机械作用在碳酸盐岩形成中占有重要位置。在浅海带中一经沉淀的碳酸盐沉积物就受到水动力带能量的改造、簸选和沉积分异,形成以机械作用为主的各种滩、坝颗粒碳酸盐沉积体。同时,波浪、潮汐流、风暴流搅动海盆地,促使海水中CO2迅速释放,由新鲜的水流带来充分的养料,加速生物繁殖,因而使碳酸盐沉积。
在有陆源输入的浅海盆地,碳酸盐沉积受到排斥和干扰,形成不纯的泥质和砂质碳酸盐岩。在有障壁的泻湖和海湾,常常因海水中Mg浓度增加,形成高镁碳酸盐岩和白云岩。在大陆淡水环境,碳酸盐过饱和时常常形成各种结壳状碳酸盐岩──钙结岩。
