物质的量
物质的量,是量度一定量粒子的集合体中所含粒子数量的物理量。物质的量是国际单位制中7个基本物理量之一。在国际单位制中,物质的量的符号为n,单位比,即n=N/NA。它是把微观粒子与宏观可称量物质联系起来的一种物理量。其表示物质所含粒子数目的多少。
-
选择特殊符号
选择搜索类型
请输入搜索
物质的量,是量度一定量粒子的集合体中所含粒子数量的物理量。物质的量是国际单位制中7个基本物理量之一。在国际单位制中,物质的量的符号为n,单位比,即n=N/NA。它是把微观粒子与宏观可称量物质联系起来的一种物理量。其表示物质所含粒子数目的多少。

NA以0.012kgC-12(请注意,此处C-12中C-12 是指原子核内有6个质子和6个中子的碳原子)所含的碳原子数作基准,其近似值为6.0221367×10^23mol^-1.1mol的任何物质所含有的该物质的微粒数叫阿伏伽德罗常数,近似值为NA=6.0221367×10^23。
注意<1>1mol任何微粒的粒子数为阿伏伽德罗常数,其不因温度压强等条件的改变而改变。
<2>应用阿伏伽德罗定律及理论(在相同的温度和压强下,相同体积的任何气体都含有相同数目的分子)时要满足:物质在所给温度,压强下为气体[1]
n=N/NA
满足上述关系的粒子是构成物质的基本粒子(如分子、原子、离子、质子、中子、电子)或它们的特定组合.
如:1molCaCl2与阿伏加德罗常数相等的粒子是CaCl2粒子,其中Ca2+为1mol、Cl-为2mol,阴阳离子之和为3mol或原子数为3mol.
在使用摩尔表示物质的量时,应该用化学式指明粒子的种类,而不使用该粒子的中文名称。例如说“1mol氧”,是指1mol氧原子,还是指1mol氧分子,含义就不明确。又如说“1mol碳原子”,是指1molC-12,还是指1molC-13,含义也不明确。
粒子集体中可以是原子、分子,也可以是离子、质子。中子。电子等。例如:1 mol F,0.5 mol CO2,1k mol CO2-3,a mol e-,1.5 mol Na2CO3·10H2O等。
1mol F中约含6.02×10^23个F原子
0.5mol CO2中约含0.5×6.02×10^23个CO2分子
1k mol CO32-(碳酸根离子)(2-为得到了两个电子而带2个单位的负电荷)中约含1000×6.02×10^23个CO32-(2-为它显负电荷)离子
a mol e-中约含a×6.02×10^23个e-
1.5 mol Na2CO3·10H2O中约含1.5×6.02×10^23个Na2CO3·10H2O,即约含有3×6.02×10^23个Na+、1.5×6.02×10^23个CO3 2-、15×6.02×10^23个H2O.
1mol 近似值为6.02×10^23摩尔质量(M) 单位 g/mol (公式M=m/n) 1.定义:单位物质的量的物质所具有的质量(1mol物质的质量)叫摩尔质量,即1mol该物质所具有相对原子质量与摩尔质量的数值等同。
物质的量(n)、质量(m)、摩尔质量(M)之间的关系为:n=m/M
2.1mol粒子的质量以克为单位时在数值上都与该粒子的相对原子质量(Ar)或相对分子质量(Mr)相等。(摩尔质量的数值与式量相同)
n=N/NA
n=m/M
n=V/Vm
平均摩尔质量
混合物利用平均摩尔质量求物质的量之比:平均摩尔质量 =混合物中各组分的摩尔质量×该组分的物质的量分数(若是气体组分可以是体积分数)。
(M1 M2表示混合物中两种物质的摩尔质量 M平均 指混合物质的平均摩尔质量)
M1-M平均 n2
—————— = ———
M平均-M2 n1
在台湾被称为物量
物质的量——n 物质的质量——m
摩尔质量——M 粒子数(微粒的个数)——N
阿伏加德罗常数——NA 相对原子质量——Ar
相对分子质量——Mr 质量分数——ω
气体摩尔体积——Vm——L/mol——22.4L/mol(在标准状况下,即在0℃101千帕的条件下)
物质的量浓度——CB(B在C的右下角)——mol/L
物质的量(mol)=物质的质量(g)/物质的摩尔质量(g/mol)
以单位体积溶液里所含 溶质B(B表示各种溶质)的物质的量来表示溶液组成的物理量,叫做溶质B的物质的量浓度。
常用单位:mol/L或mol/ m³。
气体的体积V=物质的量(mol)x气体摩尔体积(Vm)
渗透浓度定义为渗透活性物质(溶液中产生渗透效应的溶质粒子)的物质的量除以溶液的体积。物质的量浓度指的是溶质的浓度。区别在于渗透浓度是离子状态计算,物质的量浓度是以物质计算。渗透压的大小决定于全溶质粒子...
矿山开采出来的铀矿石,先要经过破碎、磨细等工序的处理,使矿石粒度达到大约0.1毫米,这样铀矿物充分暴露便于浸出。
第一类 A级无机物品(山奈)NaCN(山奈钾)KCN氰化钙Ca(CN)2氰化钡Ba(CN)2氰化钴Co(CN)2·2H2O氰化钴钾(钴)K3[Co(CN)6]氰化镍(氰化亚镍)Ni(CN)2·4H2O...

 物质的量浓度及其计算.
物质的量浓度及其计算.
物质的量浓度及其计算.
物质的量浓度及其计算.

 谷物质量流量测量装置的设计与试验
谷物质量流量测量装置的设计与试验
谷物质量流量测量装置的设计与试验
设计了一种新型冲量式谷物质量流量测量装置,该装置包括减震器、承载板、悬臂梁式弹性元件和机架等,并采用减震器来减弱收割机振动对测量精度的影响。试验证明:所设计的冲量式谷物质量流量测量装置测量误差平均值为4.29%,具有工程意义。
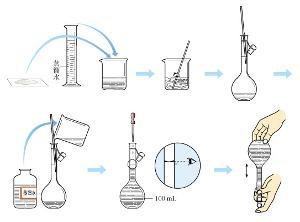
“物质的量浓度溶液的配制”内容不多,教师采用学生自主学习的方式来进行教学,给足学生足够的时间,通过学生完成实验后完成一定的课堂练习来深化教学效果。 教材是以固体NaCl为实验材料,能很好地让学生了解“物质的量浓度溶液配制”的过程”,将学生分组进行实验,从而达到更好的实验效果,完成更好的教学效果。 2100433B
高中 化学
1.一.从实验学化学/4.化学计量在实验中的应用/J.一定物质的量浓度溶液的配制。
本考点复习了以下内容: 1.物质的量浓度的概念、计算公式和特点 2.有关物质的量浓度计算的两大类型 (1)溶液中溶质的质量分数与物质的量浓度的换算。 (2)溶液稀释、同种溶质的溶液混合的计算。