电导率
- 电导率,物理学概念,也可以称为导电率。在介质中该量与电场强度E之积等于传导电流密度J。对于各向同性介质,电导率是标量;对于各向异性介质,电导率是张量。生态学中,电导率是以数字表示的溶液传导电流的能力。单位以西门子每米(S/m)表示。
-

选择特殊符号
选择搜索类型
请输入搜索

电导率的测量通常是溶液的电导率测量。固体导体的电阻率可以通过欧姆定律和电阻定律测量。电解质溶液电导率的测量一般采用交流信号作用于电导池的两电极板,由测量到的电导池常数K和两电极板之间的电导G而求得电导率σ。
电导率测量中最早采用的是交流电桥法,它直接测量到的是电导值。最常用的仪器设置有常数调节器、温度系数调节器和自动温度补偿器,在一次仪表部分由电导池和温度传感器组成,可以直接测量电解质溶液电导率。
电导率的测量原理是将相互平行且距离是固定值L的两块极板(或圆柱电极),放到被测溶液中,在极板的两端加上一定的电势(为了避免溶液电解,通常为正弦波电压,频率1~3 kHz)。然后通过电导仪测量极板间电导。
电导率的测量需要两方面信息。一个是溶液的电导G,另一个是溶液的电导池常数Q。电导可以通过电流、电压的测量得到。
根据关系式K=Q×G可以得到电导率的数值。这一测量原理在直接显示测量仪表中得到广泛应用。
而Q= L/A
A——测量电极的有效极板面积
L——两极板的距离
这一值则被称为电极常数。在电极间存在均匀电场的情况下,电极常数可以通过几何尺寸算出。当两个面积为1 cm2的方形极板,之间相隔1 cm组成电极时,此电极的常数Q=1 cm-1。如果用此对电极测得电导值G=1000 μS,则被测溶液的电导率K=1000 μS/ cm。
一般情况下,电极常形成部分非均匀电场。此时,电极常数必须用标准溶液进行确定。标准溶液一般都使用KCl溶液这是因为KCl的电导率的不同的温度和浓度情况下非常稳定,准确。0.1 mol/L的KCl溶液在25℃时电导率为12.88 mS/cm。
所谓非均匀电场(也称作杂散场,漏泄场)没有常数,而是与离子的种类和浓度有关。因此,一个纯杂散场电极是最复杂的电极,它通过一次校准不能满足宽的测量范围的需要。
电导电极一般分为二电极式和多电极式两种类型。
二电极式电导电极是国内使用最多的电导电极类型,实验式二电极式电导电极的结构是将二片铂片烧结在二平行玻璃片上,或圆形玻璃管的内壁上,调节铂片的面积和距离,就可以制成不同常数值的电导电极。通常有K=1.K=5.K=10等类型。而在线电导率仪上使用的二电极式电导电极常制成圆柱形对称的电极。当K=1时,常采用石墨,当K=0.1.0.01时,材料可以是不锈钢或钛合金。
多电极式电导电极,一般在支持体上有几个环状的电极,通过环状电极的串联和并联的不同组合,可以制成不同常数的电导电极。环状电极的材料可以是石墨、不锈钢、钛合金和铂金。
电导电极还有四电极类型和电磁式类型。四电极电导电极的优点是可以避免电极极化带来的测量误差,在国外的实验式和在线式电导率仪上较多使用。电磁式电导电极的特点是适宜于测量高电导率的溶液,一般用于工业电导率仪中,或利用其测量原理制成单组分的浓度计,如盐酸浓度计、硝酸浓度计等。
根据公式K=S/G,电极常数K可以通过测量电导电极在一定浓度的KCl溶液中的电导G来求得,此时KCl溶液的电导率S是已知的。
由于测量溶液的浓度和温度不同,以及测量仪器的精度和频率也不同,电导电极常数K有时会出现较大的误差,使用一段时间后,电极常数也可能会有变化,因此,新购的电导电极,以及使用一段时间后的电导电极,电极常数应重新测量标定,电导电极常数测量时应注意以下几点:
1. 测量时应采用配套使用的电导率仪,不要采用其它型号的电导率仪。
2. 测量电极常数的KCL溶液的温度,以接近实际被测溶液的温度为好。
3. 测量电极常数的KCL溶液的浓度,以接近实际被测溶液的浓度为好。
电导率测量是与温度相关的。温度对电导率的影响程度依溶液的不同而不同,可以用下面的公式求得:
Gt = Gtcal{1 α(T-Tcal)}
其中:
Gt = 某一温度(°C)下的电导率
Gtcal = 标准温度(°C)下的电导率
Tcal = 温度修正值
α = 标准温度(°C)下溶液的温度系数。
下表列出了常用溶液的α值。要得到其他溶液的α值,只要测量某个温度范围内的电导率,并以温度为纵轴绘出
| 溶液 (25°C) |
浓度 |
Alpha (α) |
| 盐酸 |
10 wt% |
1.56 |
| 氯化钾溶液 |
10 wt% |
1.88 |
| 硫酸 |
50 wt% |
1.93 |
| 氯化钠溶液 |
10 wt% |
2.14 |
| 氢氟酸 |
1.5 wt% |
7.20 |
| 硝酸 |
31 wt% |
31.0 |
相应的电导率的变化曲线,与标准温度相对应的曲线点为该溶液的α值。
市场上所销售的所有电导仪都可以参照标准温度(通常为25°C)进行调节的或自动温度补偿。大多数固定温度补偿的电导仪的α调节为2%/°C(近似25°C时氯化钠溶液的α)。可调节温度补偿的电导仪可以把α调节到更加接近所测溶液的α。
中国和不少国家的电导率基准是以相对测量法建立的,是一种国家副基准。
将一种纯度优于99.99%的高纯度氯化钾作为符合国际推荐的电导率基准物质,由它所配制的基准溶液应具有国际推荐电导率值。以25℃的溶液电导率为起始点,相应地测出各个电导率常数,然后按下式求出其他温度的电导率常数K
K=K0(1-at)
式中,K0为0℃下电导池常数;a为制作电导池所用玻璃线性膨胀系数;t为溶液温度,单位℃。
上式为近似推导结果,与考虑复杂情况时最多不会超过正负1xl0的差别。再根据不同温度下各溶液在相应电导池上所实测到的电阻值,相应地计算出各溶液在不同温度下的电导率。因为电导池常数相对变化的温度系数为-8.49x10℃,而KCl溶液电导率的温度系数大约为+2x10℃-。因此,假如1D、0.1D和0.01D溶液在18℃和20℃下所测得的电导率与国际推荐值-致,则可以认为这样的相对测量方法是可靠的,这在以后的国际样品比较中得到了验证。其中20℃的国际推荐值是1972年和1976年IUPAC推荐值。
电导率(conductivity)是用来描述物质中电荷流动难易程度的参数。在公式中,电导率用希腊字母σ来表示。电导率σ的标准单位是西门子/米(简写做S/m),为电阻率ρ的倒数,即σ=1/ρ。
当1安培(1 A)电流通过物体的横截面并存在1伏特(1 V)电压时,物体的电导就是1 S。西门子实际上等效于1安培/伏特。如果σ是电导(单位西门子),I是电流(单位安培),E是电压(单位伏特),则:
σ = I/E
通常,当电压保持不变时,这种直流电电路中的电流与电导成比例关系。如果电导加倍,则电流也加倍;如果电导减少到它初始值的1/10,电流也会变为原来的1/10。这个规则也适用于许多低频率的交流电系统,如家庭电路。在一些交流电电路中,尤其是在高频电路中,情况就变得非常复杂,因为这些系统中的组件会存储和释放能量。
电导和电阻也有关系,如果R是一个组件和设备的电阻(单位欧姆Ω),电导为G(单位西门子S),则:G = 1/R 。
电导率 (electric conductivity) 是表示物质传输电流能力强弱的一种测量值。当施加电压于导体的两端时,其电荷载子会呈现朝某方向流动的行为,因而产生电流。电导率 是以欧姆定律定义为电...
需要检测,是属于B类计量器具,校验周期为一年,即每年需要送质监局或其他检测机构检验。
电导率:物理学概念,也可以称为导电率。即在介质中该量与电场强度E之积等于传导电流密度J。对于各向同性介质,电导率是标量;对于各向异性介质,电导率是张量。生态学中,电导率是以数字表示的溶液传导电流的能力...
电导率与温度具有很大相关性。金属的电导率随着温度的升高而减小。半导体的电导率随着温度的升高而增加。在一段温度值域内,电导率可以被近似为与温度成正比。为了要比较物质在不同温度状况的电导率,必须设定一个共同的参考温度。电导率与温度的相关性,时常可以表达为,电导率对上温度线图的斜率。
固态半导体的掺杂程度会造成电导率很大的变化。增加掺杂程度会造成电导率增高。水溶液的电导率高低相依于其内含溶质盐的浓度,或其它会分解为电解质的化学杂质。水样本的电导率是测量水的含盐成分、含离子成分、含杂质成分等等的重要指标。水越纯净,电导率越低(电阻率越高)。水的电导率时常以电导系数来纪录;电导系数是水在 25°C 温度的电导率。
有些物质会有各向异性(anisotropy) 的电导率,必需用 3 X 3 矩阵来表达(使用数学术语,第二阶张量,通常是对称的)。
中国和不少国家的电导率基准是以相对测量法建立的,是一种国家副基准。
将一种纯度优于99.99%的高纯度氯化钾作为符合国际推荐的电导率基准物质,由它所配制的基准溶液应具有国际推荐电导率值。以25℃的溶液电导率为起始点,相应地测出各个电导率常数,然后按下式求出其他温度的电导率常数K
K=K0(1-at)
式中,K0为0℃下电导池常数;a为制作电导池所用玻璃线性膨胀系数;t为溶液温度,单位℃。
上式为近似推导结果,与考虑复杂情况时最多不会超过正负1xl0-5的差别。再根据不同温度下各溶液在相应电导池上所实测到的电阻值,相应地计算出各溶液在不同温度下的电导率。因为电导池常数相对变化的温度系数为-8.49x10-6℃-1,而KCl溶液电导率的温度系数大约为 2x10-2℃-1。因此,假如1D、0.1D和0.01D溶液在18℃和20℃下所测得的电导率与国际推荐值—致,则可以认为这样的相对测量方法是可靠的,这在以后的国际样品比较中得到了验证。其中20℃的国际推荐值是1972年和1976年IUPAC推荐值。

 多电极海水电导率测量电路
多电极海水电导率测量电路
多电极海水电导率测量电路
本文讨论了七种多电极电导率测量电路及多电极结构。分析了各种电路的测量原理,不同电极数目的电导池各个电极所完成的功能。

 电渗析器出水电导率的预测
电渗析器出水电导率的预测
电渗析器出水电导率的预测
对DSX-03型电渗析器出水电导率δ(μg/cm)与时间t(min)之间的关系进行了考查,结果显示在一定时间内两者星线性关系,其回归方程预测值与实测值相吻合。
电导率仪是适用于精密测量各种液体介质的仪器设备,主要用来精密测量液体介质的电导率值,当配以相应常数的电极可以精确测量高纯水电导率,广泛应用各领域的科研和生产。
电导率仪是实验室电导率测量仪表,它除能测定一般液体的电导率外,且能满足测量高纯水的电导率的需要。仪器有0~10mV讯号输出,可接自动电子电位差计进行连续记录。
在电解质的溶液中,带电的离子在电场的影响下,产生移动而传递电子,因此,具有导电作用。其导电能力的强弱称为电导度S。因为电导是电阻的倒数,因此,测量电导大小的方法,可用两个电极插入溶液中,以测出两个极间的电阻R。据欧姆定律,温度一定时,这个电阻与电极的间距L(cm)成正比,与电极的截面积 A(cm )反比。
1、显示方式
2、测量范围
3、分辨率
4、电极常数
5、温补范围
6、精 度
7、电流隔离输出
8、通讯接口
9、工作电源范围
10、电极安装方式
1、检查一下指针是否指零,如果不指零调节电导率仪上的调零旋钮,
2、将电导率仪调节到校正档,指针指向最大刻度,
3、按照电极常数调节旋钮,测量时调节到测量档。
1. 电极的引线不能潮湿,否则将测不准。
2. 高纯水被盛入容器后应迅速测量,否则电导率降低很快,因为空气中的溶入水里变成碳酸根离子。 3. 盛被测溶液的容器必须清洁,无离子玷污。2100433B
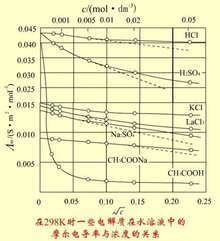
当浓度降低时,粒子之间相互作用减弱,正、负离子迁移速率加快,溶液的摩尔电导率必定升高。但不同的电解质,摩尔电导率随浓度降低而升高的程度也大不相同。当浓度降低到一定程度后,强电解质的摩尔电导率接近为一定值,而弱电解质的值仍在继续变化。
若在同一浓度区间内比较各种摩尔电导率值的变化,例如就NaCl,H2SO4,CuSO4互相比较,就会发现,当浓度降低时,各个摩尔电导率值的变化程度不同。CuSO4变化最大,H2SO4次之,而NaCl变化最小。这是因为2-2价型盐类离子之间的吸引力较大,当浓度改变时,对静电引力的影响较大,所以摩尔电导率值的变化也较大。 强电解质通常当浓度在0.001mol·dm-3以下时,Λm与√c之间呈线性关系Λm与浓度c之间有如下关系:
其中β在一定温度下,对于一定的电解质和溶剂而言是一个常数。Λm(∞)为溶液在无限稀释时的摩尔电导率,又称为极限摩尔电导率。
大气中正极性电导率()稍大于负极性电导率(),这和大气中正离子浓度大于负离子浓度的事实相吻合。大气电导率()等于正、负极性电导率之和,在海平面上,其平均值约为 2×10/(欧·厘米)(或1.8×10/秒)。此时,一个电荷为Q的孤立导体球,经过时间=1/4π(约七分半钟, 称为张弛时间)之后,其上的电荷由于传导作用将减少到 Q/e(e是自然对数的底),大约为原电量Q的37%。
大气电导率的变化和大气电场变化趋势相反,它随高度按指数律递增(见图[中、低纬度地区大气平均电导率(实线)及其极值(虚线)随高度的分布]),这是由于宇宙射线强度随高度增大、高空空气密度小而离子迁移率大等因子造成的。
