增烃水煤气水煤气和增烃水煤气对比文献

 水煤气钢管表
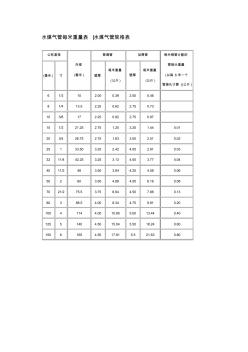
水煤气钢管表
水煤气钢管表
水煤气管每米重量表 |水煤气管规格表 公称直径 外径 (毫米 ) 普通管 加厚管 每米钢管分配的 管接头重量 (以每 6米一个 管接头计算 )(公斤 ) (毫米 ) 寸 壁厚 每米重量 (公斤 ) 壁厚 每米重量 (公斤 ) 6 1/3 10 2.00 0.39 2.50 0.46 8 1/4 13.5 2.25 0.62 2.75 0.73 10 3/8 17 2.25 0.82 2.75 0.97 15 1/2 21.25 2.75 1.25 3.25 1.44 0.01 20 3/4 26.75 2.75 1.63 3.50 2.01 0.02 25 1 33.50 3.25 2.42 4.00 2.91 0.03 32 11/4 42.25 3.25 3.13 4.00 3.77 0.04 40 11/2 48 3.50 3.84 4.25 4.58 0.06

 焦炉煤气配半水煤气生产合成氨扩能改造
焦炉煤气配半水煤气生产合成氨扩能改造
焦炉煤气配半水煤气生产合成氨扩能改造
分析了山西丰喜华瑞煤化工公司焦炉煤气配半水煤气生产合成氨18-30项目生产工艺流程,结合周边焦化厂富余焦炉煤气的实际供应情况,对原工艺流程进行优化,改造方案为:增加变压吸附提氢工序、强化甲烷转化工艺条件、增加部分设备等。通过改造,可使合成氨生产能力由18万t/a提高到24万t/a、尿素生产能力由30万t/a提高到40万t/a,取得较好的经济效益和社会效益。